Поступление кальция в клетку регулируется нейрогормональными сигналами, одни из которых увеличивают скорость вхождения Са + в клетку из межклеточного пространства, другие - высвобождение иона из внутриклеточных депо. Поскольку действие многих нестероидных гормонов на клетку опосредуется кальцием, этот элемент, наряду с циклическими нуклеотидами, считается вторичным посредником в реализации механизма действия гормонов.
Из внеклеточного пространства Са2+ попадает в клетку через кальциевый канал. Этот интегративный белок состоит из 5 субъединиц, одна из которых является собственно каналом - водной порой, образуемой гидрофильными аминокислотами. Другая представляет собой воротный механизм, открывающийся при деполяризации клетки (при поступлении Са2+). Отдельная субъединица называется метаболическими воротами, которые способны фосфорилироваться и дефосфорилироваться. Фосфорилирование осуществляется цАМФ-зависимой протеинкиназой А - следовательно, кальциевый канал активируется гормона-
ми, механизм действия которых реализуется через цАМФ. Дефосфорилирование, т.е. инактивация канала, катализируется цитоплазматической фосфата-зой (фермент состоит из 2-х субъединиц: а (61кДа) связывает калмодулин, Р (19 кДа) - Са2+, после присоединения калмодулина фосфатаза активируется).
В плазматической мембране клеток имеется ещё один кальциевый канал - лиганд-регулнруемый кальциевый канал (его лигандами являются внеклеточная АТФ, цАДФ-рибоза, лейкотриены).
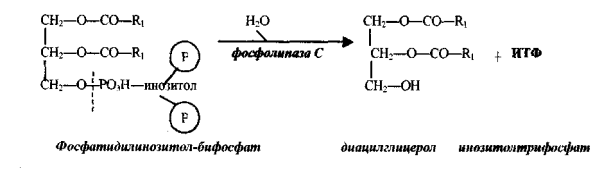
Высвобождение Са2+ из внутриклеточных депо является достаточно сложным процессом. Вначале, в ответ на нейрогормональный стимул, активируется фосфолипаза С. Этот фермент гидролизует минорный фосфолипид плазматической мембраны ФИФ2 (фосфатидилинозитол-4,5- бифосфат) на ДАТ (диацшглицерол) и ИТФ (инозитол-1,4,5-трифосфат).бифосфат) (диацшглицерол)
Эффект ИТФ и ДАТ синергичен (рис.14.1): ИТФ присоединяется к специфическому рецептору кальцисомы; конформационные изменения рецептора влекут за собой открытие ворот, запиравших канал для прохождения Са2+ из кальцисомы; высвободившийся из депо кальций связывается с протеинкина-зой С ДАГ повышает активность этой Са-зависимой протеинкиназы С.
Протеинкиназа С фосфосфорилирует различные белки (ферменты), изменяя тем самым их активность. Через фосфатидилинозитольный каскад опосредуются многие метаболические эффекты, например, гликогенолиз в печёночных клетках, высвобождение серотонина и агрегация тромбоцитов, выброс гистамина из тучных клеток, сокращение гладких мышц.
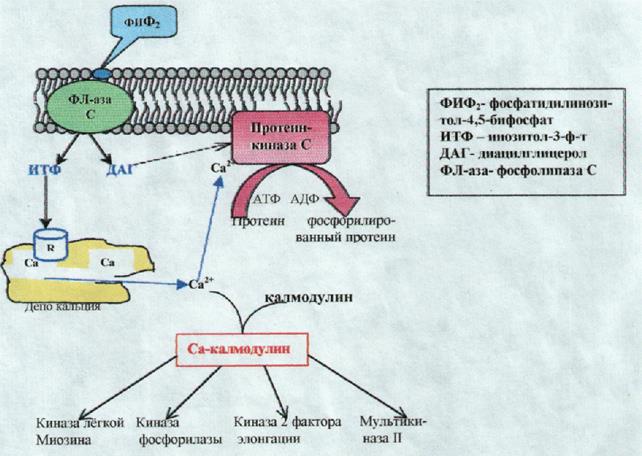
Рис. 14.1. Высвобождение Са++ из внутриклеточных депо.
Ионы кальция, поступившие в клетку извне или высвободившиеся из внутриклеточных депо, действуют 2 путями:
1. непосредственно связывают отрицательно заряженные группы на поверхности мембран, изменяя тем самым их полярность и возбудимость; кроме того, Са++ может реагировать с отрицательно заряженными группами белков, изменяя их конформацию и свойства (например, связывая СОО" группы у-карбокси-глутаминовой кислоты в составе факторов свёртывающей системы крови)
2. реализовать свой эффект с участием калмодулина. Калмодулин является частью множества Са++ - связывающих белков. Его молекулярная масса = 17000
Калмодулин имеет 2 высокоаффинных Са++ -связывающих участка на каждом из своих двух глобулярных доменов. Эти участки формируют почти совмещающиеся спиралъ-петля-спиралъ структуры, называемые EF-рукой. EF-рука - типичная пространственная организация сайтов (участков) связывания кальция во многих Са-связывающих белках.
При повышение концентрации Са2+ в клетке связывание иона с калмодулином сопровождается конформационной перестройкой последнего, приводящей к способности комплекса Са-калмодулин модулировать (отсюда такое название - «калмодулин») активность множества внутриклеточных белков: киназу лёгкой цепи миозина, киназу фосфорилазы, мультикиназу II, активирующую, в свою очередь, путём фосфорилирования ферменты синтеза углеводов (гликогенсинтазу), жирных кислот (ацетил-КоА-карбоксилазу), холестерола (ГМГ-КоА-редуктазу), фосфолипазу А2, эпидермальный фактор роста, ассоциацию микротубулина.
Выход кальция из клетки. Этот процесс осуществляется в основном 2 -мя внутриклеточными механизмами: Са++-АТФ-азой и Na+-Са++-антипортом.
Са-АТФ-аза активируется Са-калмодулиновым комплексом. Связывание кальция этим ферментом и транспорт иона через плазматическую мембрану в межклеточное пространство требует затраты энергии:
Следовательно, процесс саморегуляции внутриклеточного гомеостаза Са++ осуществляется по принципу обратной связи: выход ионов кальция в цитозоль клетки активирует калмодулин, а образовавшийся Са-калмодулиновый комплекс, активируя многочисленные ферменты, одновременно устраняет избыток кальция, ускоряя его выведение за счет активации Са++-АТФ-азы.
Na+-Са++- антипорт.. Способность клетки освобождаться от кальция связана также с функционированием Nа+/К+-АТФ-азы: поступление Na+ в клетку включает в работу механизм, ответственный за выход из неё кальция.
 2015-04-30
2015-04-30 5386
5386
