Для удобства часто вместо Ка используют рКа= ¾ lg Ка
Кислотность различных классов органических соединений с одинаковыми радикалами увеличивается в следующей последовательности:
| R – H2С – H Алканы | R-NH-H Амины | R-O-H Спирты | R-S-H Тиолы | 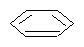 R¾ ¾ ОН
Фенолы R¾ ¾ ОН
Фенолы
| R – СOOH Карбоновые кислоты |
| рКа 50 | рКа 30 | рКа 18 | рКа 12 | pКа 10 | рКа 4,7 |
| СН кислоты | NH кислоты | ОН кислоты | SH кислоты | ОН кислоты | ОН кислоты |
Причиной самой слабой кислотности С-Н кислот является то, что углерод обладает низкой электроотрицательностью и проявляет слабую способность удерживать отрицательный заряд на анионе. Поэтому образование карбанионов является энергетически невыгодным процессом:
СН4 ® СН3 ˉ + Н+
Карбанион
(метиланион)
Среди насыщенных соединений заметную кислотность проявляют спирты (О-Н-кислоты), что обусловлено достаточной электроотрицательностью атома кислорода, т.е. способностью удерживать электронную пару в анионе, тем самым, стабилизируя его:
R ¾ O ¾ H ® R ¾ Oˉ + H+
спирт алкоксид-
анион
Стабильность аниона R – Oˉ значительно повышается с появлением возможности делокализации отрицательного заряда либо за счет электроотрицательного элемента в радикале, либо по системе сопряженных связей. Так, например, увеличение кислотности нарколана (Br3C–CH2-OH) объясняется влиянием –I эффекта трех атомов брома в радикале (стабилизирующий фактор).
 |
Увеличение кислотности фенолов по сравнению с алифатическими спиртами объясняется стабильностью фенолят-аниона, отрицательный заряд которого делокализуется по ароматическому кольцу вследствие +М эффекта.

 Br3C–CH2-OH Br3CCH2O¾ + H+
Br3C–CH2-OH Br3CCH2O¾ + H+
Тиолы проявляют более сильные кислотные свойства по сравнению со спиртами благодаря большему размеру атома серы, в котором отрицательный заряд лучше делокализуется, стабилизируя тиолятный анион.
Карбоновые кислоты в данном ряду – самые сильные кислоты.
Это объясняется образованием стабильного карбоксилат аниона при диссоциации карбоновых кислот. Карбоксилат анион стабилизирован за счет делокализации отрицательного заряда по системе сопряжения:
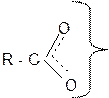
¾
Изменение основности будет противоположно изменению кислотности. Чем выше основность, тем ниже кислотность.
Спирты
Производные углеводородов, в которых один или несколько атомов водорода замещены на ОН-группы, называют спиртами. Общая формула R-O-H.
Классификация:
1) по атомности – по количеству ОН-групп на одно- и многоатомные спирты;
2)по характеру радикала – предельные и непредельные; алифатические и ароматические;
3) по характеру атома углерода, с которым связана ОН-группа, – первичные, вторичные, третичные спирты.
 2015-04-30
2015-04-30 484
484








