В многоатомных молекулах можно выделить три вида движений: электронное, колебательное и вращательное. Первое связано с движением электронов вокруг ядер атомов, второе — с периодическим изменением расстояний между ядрами, третье — с периодическим изменением ориентации молекул в пространстве. В соответствии с видами движений энергия молекулы приблизительно может быть представлена в виде суммы энергий электронной, колебательной и вращательной:
 E=Eэл+Eкол+Eвр(1.6)
E=Eэл+Eкол+Eвр(1.6)
По значению слагаемые в формуле (1.6.) различаются между собой: Еэл ~ 1 эВ, Екол ~ 102 эВ, Евр ~ 104 эВ. Энергия молекулы квантуется. Возможные значения энергии определяются внутренним строением самой молекулы. Электронные состояния, обозначенные буквами S, P, D, …., характеризуются определенными уровнями электронной энергии 0, 1, 2,... (рис.1.3). Самому нижнему, нулевому уровню соответствует основное, невозбужденное состояние, всем остальным уровням — возбужденные состояния. Переходам из основного состояния в возбужденные (рис.1.3, переходыизображены стрелками) соответствуют поглощения энергии молекулой, обратным переходам — выделение энергии.
В каждом электронном состоянии возможно несколько разных колебаний (рис.1.3, колебательные уровни v0, v1, v2,..., v’0, v’l, v’2). В каждом электронно-колебательном состоянии возможны различные вращения (рис. 1.3, вращательные уровни j0, jl, j2,..., j’0, j’l, j’2,...).
При переходе молекулы из одного состояния в другое энергия молекулы меняется. Если переход сопровождается испусканием, то энергия кванта излучения равна:
hn=E’-E= (E’эл-Eэл)+ (E’кол-Eкол)+(E’вр-Eвр),(1.7.)
где h — постоянная Планка; n — частота излучения; Е' и Е — энергии верхнего и нижнего энергетических уровней молекулы; Е'эл, Е’кол, Е'вр и Еэл, Екол, Евр —электронная, колебательная и вращательная энергии молекулы в возбужденном и основном состояниях соответственно. При таком переходе получаются электронно-колебательно-вращательные спектры (их называют электронными).
Если при изменении состояния молекулы величина DЕэл=0, а DЕкол¹0 и DЕвр¹0, то возникают колебательно-вращательные спектры (их называют колебательными). Если изменяется только вращательная энергия (DЕэл=0, а DЕкол=0 и DЕвр¹0), то возникают вращательные спектры.
Число различных колебательных переходов, сопровождающих электронный переход, и различных вращательных переходов, сопровождающих колебательный переход, весьма велико. Поэтому наблюдается сложная структура молекулярных спектров. Молекулярные спектры сплошные. Распределение интенсивности в спектре испускания (или поглощения) зависит от структуры энергетических уровней, их населенности и вероятностей переходов между различными уровнями энергии. Так как DЕэл>DЕкол> DЕвр, то при изучении электронных спектров вращательной структурой спектров можно пренебречь.
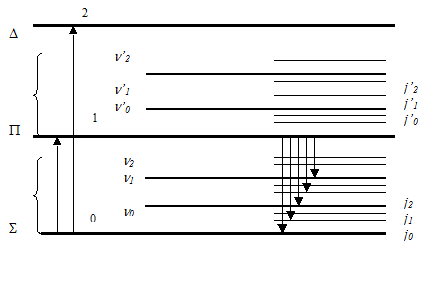
Рис. 1.3. Схема энергетических уровней молекулы.
1.4. Эмиссионный и абсорбционный спектральный анализ, его медицинское применение.
Спектры поглощения и испускания вещества являются источником информации о качественном составе (из каких молекул или атомов состоит вещество), количественном соотношении различных компонентов вещества, их состоянии и структурной организации.
В спектральном анализе используют как спектры испускания (эмиссионный спектральный анализ), так и спектры поглощения (абсорбционный спектральный анализ).
В зависимости от энергии (частоты) фотона, испускаемого или поглощаемого атомом (или молекулой), классифицируют следующие виды спектроскопии: радио-, ИК-, УФ-, видимого излучения, рентгеновская.
По типу вещества источника спектра различают атомные, молекулярные спектры и спектры кристаллов.
В медицинских целях эмиссионный анализ служит в основном для определения микроэлементов в тканях организма, небольшого количества атомов металлов в консервированных продуктах с гигиенической целью, некоторых элементов в трупных тканях для целей судебной медицины и так далее.
Абсорбционные спектры широко используются в современных биохимических и биофизических работах.
Различают качественный (определение состава вещества) и количественный (определение концентраций соединений, входящих в данное вещество) спектральный анализ.
 2015-05-14
2015-05-14 1796
1796








