Согласно стандарту ISO 8044-1986 ингибиторами коррозии (ИК) называют химические соединения, которые, присутствуя в коррозионной системе в достаточной концентрации, уменьшают скорость коррозии без значительного изменения концентрации любого коррозионного реагента. Ингибиторами коррозии могут быть и композиции химических соединений. Содержание ингибиторов в коррозионной среде должно быть небольшим.
Эффективность ингибиторов оценивается степенью защиты Z (в %) и коэффициентом торможения γ (ингибиторный эффект) и определяется по формулам:
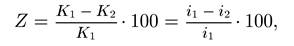

Коэффициент торможения показывает во сколько раз уменьшается скорость коррозии в результате действия ингибитора:
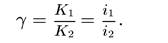
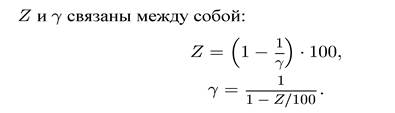
Ингибиторы подразделяются:
• по механизму своего действия — на катодные, анодные и смешанные;
• по химической природе — на неорганические, органические и летучие;
• по сфере своего влияния — в кислой, щелочной и нейтральной среде.
Действие ингибиторов обусловлено изменением состояния поверхности металла вследствие адсорбции ингибитора или образования с катионами металла труднорастворимых соединений. Защитные слои, создаваемые ингибиторами, всегда тоньше наносимых покрытий.
Ингибиторы могут действовать двумя путями: уменьшать площадь активной поверхности или изменять энергию активации коррозионного процесса.
В результате адсорбции ингибитора происходит изменение структуры двойного электрического слоя. Катодные и анодные ингибиторы замедляют соответствующие электродные реакции, смешенные ингибиторы изменяют скорость обеих реакций. Адсорбция и формирование на металле защитных слоев обусловлены зарядом частиц ингибитора и способностью образовывать с поверхностью химические связи. Катодные ингибиторы замедляют катодные реакции или активное растворение металла. Для предотвращения локальной коррозии более эффективны анионные ингибиторы. Часто для лучшей защиты металлов используют композиции ингибиторов с различными добавками. При этом может наблюдаться:
• аддитивное действие, когда ингибирующий эффект отдельных составляющих смеси суммируется;
• антагонизм, когда присутствие одного из компонентов ослабляет ингибирующее действие другого компонента;
• синергизм, когда компоненты композиции усиливают ингибирующее действие друг друга.
Влияние ингибиторов на коррозию можно оценить сравнением скоростей коррозионного процесса в отсутствии и в присутствии ингибитора.
Способностью замедлять коррозию металлов в агрессивных средах обладают многие неорганические вещества. Ингибирующее действие этих соединений обуславливается присутствием в них катионов (Са2+, Zn2+, Ni2+, As3+, Bi3+, Sb3+) или анионов (CrO42-, Cr2O72-, NO2, SiO32-, PO43-).
Неорганические катодные ингибиторы ограничивают скорость коррозии металлов путем повышения перенапряжения катодного процесса и сокращения площади катодных участков.
Экранирующие катодные ингибиторы — это соединения, которые образуют на микрокатодах нерастворимые соединения, отлагающиеся в виде изолирующего защитного слоя. Для железа в водной среде такими соединениями могут быть ZnSO4, ZnCl2, а чаще Са(НСО3)2.
Бикарбонат кальция Са(НСОз)2 — самый дешевый катодный экранирующий ингибитор, применяемый для защиты стали в системах водоснабжения. Бикарбонат кальция в подщелоченной среде образует нерастворимые соединения СаСОз, осаждающиеся на поверхности, изолируя ее от электролита.
Катодные ингибиторы, повышающие перенапряжение катодного процесса, применяются в тех случаях, когда коррозия протекает с водородной деполяризацией. В качестве ингибиторов применяют соли, содержащие катионы некоторых тяжелых металлов (AsCl3, Bi(SO4)3).
Анодные неорганические ингибиторы образуют на поверхности металла тонкие (~ 0,01 мкм) пленки, которые тормозят переход металла в раствор. К группе анодных замедлителей коррозии относятся химические соединения — пленкообразователи и окислители, часто называемые пассиваторами.
Катодно-анодные неорганические ингибиторы, например KJ, КВr в растворах кислот, тормозят в равной степени анодный и катодный процессы за счет образования на поверхности металла хемосорбционного слоя.
Пленкообразующие ингибиторы защищают металл, создавая на его поверхности фазовые или адсорбционные пленки. В их число входит NaOH, Na2CO3 и фосфаты. Наибольшее распространение получили фосфаты, которые широко используют для защиты железа и стали в системе хозяйственных и коммунальных стоков.
В присутствии фосфатов на поверхности железа образуется защитная пленка. Она состоит из гидроксида железа, уплотненного фосфатом железа. Для большего защитного эффекта фосфаты часто используются в смеси с полифосфатами. Пассиваторы тормозят анодную реакцию растворения металла благодаря образованию на его поверхности оксидов:
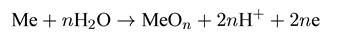
Эта реакция может протекать только на металлах, склонных к пассивации.
Пассиваторы являются хорошими, но опасными ингибиторами. При неверно выбранной концентрации, в присутствие ионов С1- или при несоответствующей кислотности среды, они могут ускорить коррозию металла, и в частности вызвать очень опасную точечную коррозию.
Защитное действие нитритов состоит в образовании поверхностной оксидной пленки по уравнению:
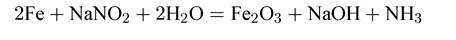
Силикаты относятся к ингибиторам смешанного действия, уменьшая скорости как катодной, так и анодной реакций. Общая формула силикатов — xSiO2·Me2O. Действие силикатов состоит в нейтрализации растворенного в воде углекислого газа и в образовании защитной пленки на поверхности металла. Пленка не имеет постоянного состава.
Полифосфаты — растворимые в воде соединения метафосфатов общей формулы (МеРО3)n- Защитное действие полифосфатов состоит в образовании непроницаемой защитной пленки на поверхности металла.
Многие органические соединения способны замедлить коррозию металла. Органические соединения — это ингибиторы смешанного действия, т.е. они воздействуют на скорость как катодной, так и анодной реакций.
Органические ингибиторы адсорбируются только на поверхности металла. Продукты коррозии их не адсорбируют. Поэтому эти ингибиторы применяют при кислотном травлении металлов для очистки последних от ржавчины, окалины, накипи. Органическими ингибиторами коррозии чаще всего бывают алифатические и ароматические соединения, имеющие в своем составе атомы азота, серы и кислорода.
Амины применяют как ингибиторы коррозии железа в кислотах и водных средах.
Тиолы (меркаптаны), а также органические сульфиды и дисульфиды проявляют более сильное ингибирующее действие по сравнению с аминами. Основные представители этого класса—тиомочевина, бензотриазол, алифатические меркаптаны, дибензилсульфоксид.
Органические кислоты и их соли применяют как ингибиторы коррозии железа в кислотах, маслах и электролитах, а также как ингибиторы процесса наводороживания. Наличие в органических кислотах амино- и гидроксильных групп улучшает из защитные свойства. Среди этой группы особенно выделяют бензоат натрия. Спирты, особенно многоосновные — эффективные ингибиторы
коррозии.
В щелочных средах ингибиторы используются при обработке амфотерных металлов, защите выпарного оборудования, в моющих составах, для уменьшения саморазряда щелочных источников тока.
Из ингибиторов для нейтральных сред следует выделить группу ингибиторов для систем охлаждения и водоснабжения. Видное место здесь занимают полифосфаты, поликарбоксильные аминокислоты, так называемые комплексоны — ЭДТА, НТА и др.; и их фосфорсодержащие аналоги — ОЭДФ, НТФ, ФБТК. Комплексоны защищают металлы только в жестких водах, где они образуют соединения с катионами Са2+ и Mg2+.
Летучие ингибиторы являются современным средством защиты от атмосферной коррозии металлических полуфабрикатов и готовых изделий на время их хранения и транспортировки. Принцип действия летучих ингибиторов коррозии заключается в образовании паров, которые диффундируют через слой воздуха к поверхности металла, и защищают ее.
В последние годы видное место заняли ингибированные восковые составы. Объединяя в себе полезные качества тонкопленочных покрытий и масел, они формируют на поверхности металлов тонкие пластичные пленки. Наличие в них ингибиторов в совокупности с гидрофобностью воска обеспечивает сильный эффект антикоррозионного последействия.
 2015-05-14
2015-05-14 3273
3273







