1924 жылы француз физигі де Бройль жарықтың екі жақтылық табиғатына, заттың екі жақтылық табиғаты сәйкес келуі керек, яғни зат бөлшектерінің тек түйіршіктік қасиеті ғана емес, олардың толқындық қасиеті болуы керек деген болжам айтты.
Кванттық механикада бөлшектің күйін толқындық функциямен сипаттайды. Толқындық функция — координаталар мен уақыттың комплекстік функциясы, оның айқын түрі Шредингер теңдеуінің шешуінен шығады да, соңында бөлшекке әрекет ететін күштердің сипатымен анықталады
Бұл қатынастарға қарағанда, мысалы, координаттың 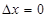 \ дәл мәні болса, онда импульстің белгілі мәні болмайды, (себебі
\ дәл мәні болса, онда импульстің белгілі мәні болмайды, (себебі 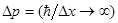 \ сондай-ақ импульстің
\ сондай-ақ импульстің 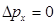 дәл мәні болса, координатаның белгілі мәні болмайды (себебі
дәл мәні болса, координатаның белгілі мәні болмайды (себебі 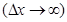 ).
).
Билет
.Кез-келген электр тогының немесе қозғалыстағы зарядталған бөлшектердің айналасында магнит өрісі болады. Магнит өрісін сандық сипаттау үшін физикалық векторлық шама магнит өрісінің индукция векторы енгізілген. Магнит өрісінің индукция векторы магнит өрісінің күштік сипаттамасы болып табылады. Өлшем бірлігі 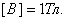 Бағыты мен шамасы өзгермейтін магнит өрісін біртекті магнит өрісі деп атайды.
Бағыты мен шамасы өзгермейтін магнит өрісін біртекті магнит өрісі деп атайды.
| Магнит өрісін көрнекті түрде бейнелеу үшін магнит өрісінің күш сызықтары немесе индукция сызықтары енгізілген. Әрбір нүктесіне жүргізілген жанама сол нүктедегі индукция векторының бағытымен сәйкес келетіндей магнит өрісінде жүргізілген сызықтарды магнит өрісінің күш сызықтары деп атайды. Күш сызықтарының жиілігі – магнит өрісінің шамасына тура пропорционал. Магнит өрісінің индукция векторының бағыты бұрғы ережесімен анықталады. Магнит өріс3нің күш сызықтары | |
тұйықталған сызықтар, яғни магнит өрісі – құйынды өріс болып табылады.Тұрақты магнитте екі полюс болады. Оның солтүстік полюсін - N, оңтүстік полюсін - S деп белгілейді. Тұрақты магниттің магнит өрісі оңтүстік полюстен солтүстік полюске қарай бағытталады. Соленоид (грекше solen – түтік және іdos – түр) – ток жүретін оқшауланған сымнан оралған цилиндр тәрізді индуктивті орама. Соленоидтың ішкі қуысының орта бөлігінде (ұзындығы Соленоид диаметрінен едәуір үлкен) магнит өрісі соленоид осінепараллель бағытталады және біртекті әрі бұл өрістің кернеулігі ток күшіне және орам санына (жуық шамамен) пропорционал болады. Соленоид тың сыртқы магнит өрісі сырықты магниттің өрісіне ұқсас. Ішкі қуысында темір өзекшесі бар соленоид электрмагнит болып есептеледі. 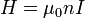 (СИ), (СИ), |
Фазалық тепе-теңдік — термодинамикалық тепе-теңдіктегі фазалардың бір мезгілде көп фазалық жүйеде болуы. Магниттелу осі бірдей, магниттелгіштігінің бағыты әр түрлі ферромагнетиктің екі фазасы (сыртқы магнит өрісі болмағанда), сыртқы магнит өрісіндегі металдың қалыпты және асқын өткізгіштік фазалары, т.б. тепе-теңдікте бола алады. Тепе-теңдік жағдайда бөлшек бір фазадан екінші фазаға ауысқанда жүйе энергиясы өзгермейді, яғни әрбір құраушының әр түрлі фазалардағы химиялық потенциалдары бірдей болады. Бұдан Гиббстің фазалар ережесі шығады. Мысалы, екі құраушы жүйенің үш фазасы әр түрлі температура кезінде тепе-теңдікте бола алады. Бірақ құраушылардың қысымы мен концентрациясы толықтай берілген температурамен анықталады. Қысым шексіз аз өзгеретін фазалық ауысу кезіндегі (қайнау, балқу, т.б.) температураның өзгерісі Клапейрон-Клаузиус теңдеуімен анықталады. Фазалық тепе-теңдік жағдайларында бір термодинамикалық айнымалы шамалардың екінші термодинамик. айнымалы шамаларға тәуелділігін кескіндейтін графиктер тепе-теңдік сызықтары, ал олардың жиынтығы күй диаграммалары деп аталады. Қатты денелерде термодинамик. тепе-теңдікке келтіретін диффузия процестерінің баяулығынан тепе-тең фазалармен қатар тепе-тең емес фазалар пайда болады. Бұл жағдайда фазалар ережесі орындалмауы мүмкін. Фазалар ережесі фазалар бір-бірінен өзгешеленетін сындар нүктеде орындалмайды. Бөлшектердің арасында алыстан әсер ететін күштер болмайтын көлемді үлгілерде тепе-тең фазалар арасындағы шекара мейлінше аз болады. Фазалардың бөліну шекарасының пішіні беттік энергияның ең аз болу шартымен анықталады.
Газ молекулаларының өзара әрекеттесу күштері
Температураның өзгеруіне байланысты зат үш түрлі күйде: қатты, сұйық және газ күйлерінде бола алады. Әр түрлі күйдегі заттың қасиеттері де түрліше болады. Бөлме температурасында (+20°С) сынаптан өзге металдар қатты күйде болса, ауадағы көптеген газдар қатты күйге минус (-270°С) температура шамасында ауысады. Жер бетінде температура негізінен +40°С-дан -50°С-ка дейін ауытқиды. Мұндай температурада азот, оттегі, сутегі сияқты заттар тек газ күйінде болатындықтан, оларды газдар деп атап кеткен. Ал газ да өте төменгі температурада сұйық және қатты күйге өте алады. Мысалы, Жерге карағанда Күннен әлдеқайда алыс орналаскан Сатурн, Уран,Нептун планеталары жағдайында жоғарыда аталған газдар сұйық және қатты күйде болады. Ол планеталарда температура өте төмен шамаға (-270°С) жетеді. Бөлме температурасында сынап буланады, ал -30°С-та қатады. Сұйық сынап, әсіресе, оның буы денсаулыққа аса қауіпті. Сондықтан сынабы бар аспаптармен жұмыс жасағанда айрыкша сақтық керек. Егер сынапты төгіп алғандай жағдай туса, міндетті түрде арнаулы қызмет орындарына айтып, кауіпсіздендіру шараларын шұғыл жүргізу қажет.
ВАН-ДЕР-ВААЛЬС ТЕҢДЕУІ және қысымы p болатын көлемі V газдың молі үшін В.-д.-В. т. мына түрде жазылады: (p + a/V2)(V—b)= =RT, мұндағы R —T— нақты (реал) газдардың күйін сипаттайтын алғашқы теңдеулердің бірі. 1873 ж. голланд физигі Я.Д. Ван-дер-Ваальс ұсынған. Темп-расы әмбебап газ тұрақтысы, а және b — нақты газ қасиеттерінің идеал газ қасиеттерінен ауытқуын көрсететін тәжірибелік тұрақтылар. Ал a/V2 — молекулааралық өзара әсердің нәтижесінде пайда болатын молекулалар арасындағы тартылысты ескеретін мүше (өлшемділігі — қысым), b — молекулалардың бір-біріне жақын келген кездегі тебілісін ескере отырып, олардың (молекулалардың) меншікті көлеміне ендірілетін түзету. Көлем (V) үлкен болған жағдайда (сондай-ақ, сиретілген газдар үшін де) a және b тұрақтыларын ескермеуге болады да В.-д.-В. т. идеал газ күйінің теңдеуіне ауысады; қ. Клапейрон теңдеуі. [1]
Ван-дер-Ваальс изотермалары – бір моль газ үшін Ван-дер-Ваальс теңдеуімен анықталатын температураның Т берілген мәндеріндегі қысымның р молярлық көлемге Vm тәуелділік қисықтары.
Эффе́ктом Джо́уля — То́мсона называется изменение температуры газа при адиабатическом дросселировании — медленном протекании газа под действием постоянного перепада давлений сквозь дроссель (пористую перегородку). Данный эффект является одним из методов получения низких температур.
Қандайда бір 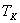 - критикалық температурада изотермада тек қана бір майысу нүктесі болады (бұл нүктеде оған жүргізілген жанама абсцисса осіне параллель). К нүктесі - критикалық нүкте, ал осы нүктеге сәйкес келетін
- критикалық температурада изотермада тек қана бір майысу нүктесі болады (бұл нүктеде оған жүргізілген жанама абсцисса осіне параллель). К нүктесі - критикалық нүкте, ал осы нүктеге сәйкес келетін 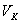 көлемі және
көлемі және 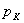 қысымдары да критикалық деп аталады.
қысымдары да критикалық деп аталады. 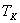 кезіндегі изотермакритикалық изотерма деп аталады.
кезіндегі изотермакритикалық изотерма деп аталады.
Нақты газдардың ішкі энергиясы 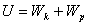 өрнегімен анықталады, мұндағы
өрнегімен анықталады, мұндағы 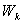 - молекулалардың қосынды кинетикалық энергиясы,
- молекулалардың қосынды кинетикалық энергиясы, 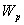 -молекулалардың қосынды өзара әсерлесу энергиясы.
-молекулалардың қосынды өзара әсерлесу энергиясы. 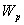 энергиясын анықтайық. Ол үшін молекулалардың арасындағы тартылу күшінің жұмысы
энергиясын анықтайық. Ол үшін молекулалардың арасындағы тартылу күшінің жұмысы 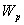 энергиясының кемуіне тең екенін ескереміз, яғни
энергиясының кемуіне тең екенін ескереміз, яғни 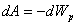 . Молекулалардың арасындағы тартылу күші
. Молекулалардың арасындағы тартылу күші 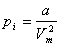 ішкі қысыммен сипатталады. Сондықтан
ішкі қысыммен сипатталады. Сондықтан 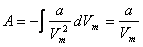 және
және 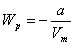 .
.
Молекулалардың қосынды 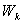 кинетикалық энергиясы олардың қозғалысына тәуелді болады.
кинетикалық энергиясы олардың қозғалысына тәуелді болады.
Билет
Магниттік момент [1] — заттың магниттік қасиеттерін сипаттайтын негізгі шама. Электр-магниттік құбылыстардың классикалық теориясына сәйкес магнетизмнің (Магниттік моменттің) көзі электр макротоктар және микротоктар (атомдық) болып табылады. Магнетизмнің қарапайым көзі ретінде тұйық ток алынады. Электр-магнит өрістің классикалық теориясы және тәжірибелік деректер бойынша тұйық токтың (тогы бар контурдың) магнит әсері ток күші (і) мен контур ауданының (s) көбейтіндісі (М) белгілі болғанда ғана анықталады:
Максвелл теориясында электродинамиканың негізгі есебі шешілді, яғни берілген зарядтар мен токтар жүйесінің тудыратын электромагниттік өрісінің сипаттамалары анықталады. Максвелл теориясы макроскопиялық теория болып табылады, яғни бұл теорияда заттардың немесе орталардың ішкі құрылыстары қарастырылмайды.
Максвелл теориясы негізінен 4 теңдеуден тұрады және әр теңдеу 2 түрде: интегралдық және дифференциалдық түрде беріледі.
Максвелдің дифференциалдық теңдеулері интегралдық теңдеулерінен векторлық анализдің екі теоремалары: Гаусс теоремасы және Стокс теоремаларының көмегімен алынады.
Бұл жағдайда Максвелл электромагниттік индукция заңын қарастырды. Уақыт өтуімен өзгеретін айнымалы магнит өрісі өзін қоршаған кеңістікте құйынды электр өрісін тудырады.
Тұйық бет арқылы өтетін кернеулік векторының циркуляциясы осы бетпен шектелген беттегі магнит өрісінің индукция векторының теріс таңбамен алынған өзгеру жылдамдығына тең болады.
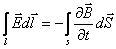
Бұл өрнек Максвелдің интеграл түріндегі I- теңдеуі деп аталады.
Атом ядросы ашылғаннан кейін оның құрылымы қандай деген мәселе қойылды. 1919 ж. Э. Резерфорд α-бөлшектермен жасаған тәжірибелерін жалғастыра отырып, ядроның құрамына кіретін бірінші бөлшекті ашты.
Жабық ыдыс ішінде α-бөлшекті шығарушы элемент Ra радий және мырыш сульфидімен қапталған мөлдір Э экран бар (8.3-сурет). Жабық ыдыстан ауа сорылып шығарылған. α-бөлшектер экранға соқтығысып, жарқылдар туғызған. Ол жарқылдарды М микроскопарқылы бақылаған. Келесі экспериментте ыдысты азот газымен толтырады. Енді а-бөлшектер өзінің энергиясын азоттың атомдарыниондауға және оларды қоздыруға жұмсап, экранға жете алмайды. Дегенмен, сирек болса да, экранда жарқылдар байқалған. Ионданукезінде пайда болатын электрондар ондай жарқылдарды туғыза алмайды. Ендеше α-бөлшек азот атомымен соқтығысқанда оның ядросынан белгісіз бір зарядталған бөлшекті ұшырып шығарған.
Изотоптар - Ядроларында протондар саны бірдей, бірақ массалары әртүрлі белгілі бір элементті құрайтын атомдар түрі. Бір ғана элементтің әртүрлі изотоптарына тән атомдар өздерінің ядросына кіретін нейтрондар саны жағынан, ядролық қасиеттері тұрғысынан бір-бірінен анық өзгешеленеді, алайда олар, электронды қабаттарықұрылысының бірдей болуына байланысты, бір-біріне өте ұқсас химиялық қасиеттерді иемденеді. Химиялық элементтердің көпшілігі атомдық салмақтары әр түрлі изотоп қоспасынан тұрады. Изотоптардың өмір сүру кезеңі секундтың мыңнан бір бөлігінен бірнеше миллион жылдарға дейін созылады Бүгінгі танда 264 тұрақты изотоптар, 50 шамалы табиғи радиоактивті изотоптар және 1000-нан астам жасанды радиоактивті изотоптар белгілі.[1]
Атом ядросының негізгі сипаттамаларының бірі оның электр заряды болып табылады. Атом ядросының зарядын алғаш рет 1913 жылыГ.Мозли өлшеген. Ал ядроның зарядын тікелей өлшеуді ағылшын физигі Дж.Чедвик 1920 жылы жүзеге асырды. Атом ядросының заряды элементар электр зарядының Менделеев кестесіндегі химиялық элементтің 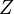 реттік нөміріне көбейтіндісіне тең болады:
реттік нөміріне көбейтіндісіне тең болады:
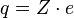 .
.
Сонымен, Менделеев кестесіндегі химиялық элементтің реттік нөмірі кез келген элемент атомының ядросындағы оң зарядтардың санымен анықталады. Сондықтан элементтің 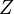 реттік нөмірін зарядтық caн деп атайды.[1]
реттік нөмірін зарядтық caн деп атайды.[1]
Атом ядросының массасы
Атом ядросының физикалық қасиеттері оның зарядымен қатар массасымен де анықталады. Ядроны сипаттайтын шамалардың ең маңыздыларының бірі — масса. Ядролық физика иондар мен атом ядросының массасын көбінесе масс-спектрографтың көмегімен анықтайды. 8.2-суретте масс-спектрографтың сұлбасы келтірілген.
Байланыс энергиясының шамасы бөлшектер арасындағы өзара әсерге байланысты анықталады. Егер бөлшектер жиынтығы молекулақұрайтын атомдар болса, онда Байланыс энергиясы ретінде химикалық байланыстың, ал бөлшектер жиынтығы ядро құрайтыннуклондар (протондар мен нейтрондар) болса, онда ядролық байланыстың энергиясы қарастырылады.
Байланыс энергиясы — теріс таңбалы шама. Өйткені байланысқан жүйенің түзілуі кезінде энергия бөлініп шығады. Байланыс энергиясының абсолют шамасы жүйе байланысының беріктілігін және жүйенің орнықтылығын сипаттайды. Басқаша айтқанда, Байланыс энергиясы артқан сайын жүйе берік болады, яғни жүйені оны құрайтын бөлшектерге жіктеу үшін жұмсалатын энергия да көп болады. Мысалы, молекулалардың химикалық Байланыс энергиясы бірнеше эВ болса, ядролық Байланыс энергиясы миллиондаған эВ-қа дейін жетеді. Сондықтан атом ядросы өте берік жүйе болып есептеледі.
23 вариант
 2015-05-20
2015-05-20 1752
1752








