Результаты измерений заносят в таблицу, обращая внимание на диапазон измерений и размерность величины. Значения молярной электропроводности λ (См·см2·моль-1) вычисляют по формуле
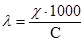 ,
,
где λ (См·см2·моль-1), χ (См·см-1), С (моль/л).
Таблица.
Результаты измерений и данные для построения графика зависимости молярной электропроводности раствора сильного электролита NaCl от концентрации.
| № | С, моль/л | χ, mS/см мили См∙см–1 | l, См∙см2∙моль–1 | √С |
| 0,1 | ||||
| 0,08 | ||||
| 0,06 | ||||
| 0,04 | ||||
| 0,02 | ||||
| 0,01 |
Строят график в координатах l от  (на миллиметровой бумаге или как результат компьютерного построения), из графика определяют l¥эксп
(на миллиметровой бумаге или как результат компьютерного построения), из графика определяют l¥эксп
l¥ эксп =
Абсолютная ошибка опыта(Δλ∞) и относительная (w%) ошибка определения l¥. Значение l¥теор вычисляют по табличным данным как сумму l¥ катиона и аниона:
l¥ теор = l¥ Na+ + l¥ Cl- = …
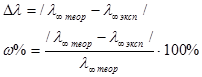
ЛАБОРАТОРНАЯ РАБОТА № 4
Тема: ОПРЕДЕЛЕНИЕ КОНСТАНТЫ ДИССОЦИАЦИИ СЛАБОГО ЭЛЕКТРОЛИТА НА ОСНОВАНИИ ЗАВИСИМОСТИ ЭЛЕКТРОПРОВОДНОСТИ ОТ КОНЦЕНТРАЦИИ.
Литература: Лекция №6; [1]: С. 283-300.
Цель: приобретение навыков измерения электропроводности раствора при помощи цифрового кондуктометра, определение константы диссоциации слабого электролита на основании зависимости электропроводности от концентрации кондуктометрическим методом.
Реактивы и оборудование:
Кондуктометр цифровой с электродом, раствор CH3COOH 0,5 моль/л; вода дистиллированная, бюретка объемом 50 мл, воронка, стакан объемом 50 мл (под бюретку), пронумерованные мерные колбы объемом 100 мл с пробкой — 4 штуки, высокий стакан объемом 150 мл для измерений электропроводности.
 2015-05-10
2015-05-10 292
292








