Движение по клеточному циклу вызывается активацией двух ключевых регуляторных киназ - CDK4 и CDK2, ассоциированных с циклинами D и Е. Фосфорелирование этими киназами белков-мишеней приводит к переходу клетки в фазу S, что требует одновременной инактивации ингибиторов, таких как RB (ретинобластома) и активации киназ-промоторов S-фазы, таких как CDC45. Онкоген myc может служить в этой системе транскрипционным фактором, и одновременно с RB, повышать количество и активность комплекса циклин Е-CDK2 киназы, который приводит к инициации репликации путем конечной активации CDC45-киназы. Именно комплекс циклин Е-CDK2 киназа является мишенью двух ветвей процесса, индуцированного повреждениями ДНК и приводящего к задержке клеточного цикла в фазе G1.
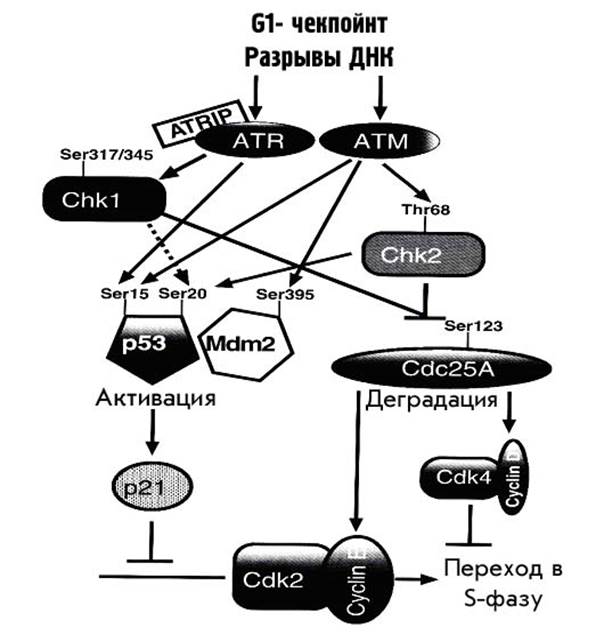
Все это подробно показано на рис. 41. G1-чекпойнт при повреждении ДНК имеет две различающиеся по своей кинетике ветви. Причем обе фазы реакции используют ATM/ATR и CHK1/CHK2 киназы.
Первая, острая фаза реакции направлена на то, чтобы заблокировать циклин Е- CDK2-киназу в неактивном состоянии, что достигается ингибированием или протеосомной деградацией фосфатазы CDC25. Затем следует более длительный и глубокий G1-арест, также связанный с инактивацией комплекса циклин Е- CDK2 киназа, что достигается благодаря стабилизации белка Р53 и его последующей – относительно более медленной – работе как транскрипционного фактора, активирующего синтез соответсивующих белков, в первую очередь - Р21. Вероятно, именно и только Р21 является мишенью Р53, важной для G1-чекпойнта при повреждении ДНК. Одновременно различными путями разрушается комплекс между Р53 и его ингибитором MDM2, что также усиливает эту реакцию. Последующая активация транскрипции MDM2, опосредованная тем же Р53, является дополнительным путем регуляции активности Р53.
Хотя бытует представление, что чекпойнты после повреждения ДНК нужны для репарации, но нет никаких данных, что G1-чекпойнт как-либо способствует репарации двунитевых разрывов. Вероятнее всего, роль G1-чекпойнта в поддержании клеточной стабильности в том, что путем Р53-опосредованного апоптоза элиминируются клетки, содержащие ДНК-повреждения.
 2015-05-10
2015-05-10 581
581








