"КАЧЕСТВЕННЫЕ РЕАКЦИИ НА НЕКОТОРЫЕ ФЕРМЕНТЫ"
Качественно ферменты можно обнаружить по их действию на те или иные субстраты.
Опыт №1. Определение пепсина.
Общие понятия.
Пепсин и химозин вырабатываются стенками желудка и катализируют реакцию гидролиза белка до пептонов. Оба фермента действуют в сильно-кислой среде (рН=1,4 – 2,5). Активатором этих ферментов является соляная кислота.
Реактивы: пепсин 1% р-р.
Исследуемое вещество: молоко (белок молока).
Ход работы: В две пробирки наливают по 2 мл молока, затем и первую пробирку добавляют 5 капель пепсина, во вторую пробирку 5 капель предварительно прокипяченного и охлажденного пепсина. Обе пробирки помещают в баню при 37°. Через несколько минут сравниваем содержимое пробирок.
Что наблюдаете? Сделайте вывод.
Опыт № 2. Реакции на тирозиназу.
Общие понятия.
Фермент тирозиназа относится к фенолооксидазам. Этот фермент катализирует окисление тирозина и других производных фенолов газообразным кислородом воздуха с образованием красного пигмента галохрома, который затем превращается в темный пигмент, родственный меланинам.
Схематично катализируемый процесс можно изобразить следующим образом:
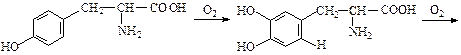
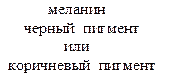
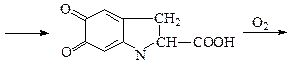
красный пигмент
Источником фермента могут быть растительные и животные ткани, например, сырой картофель, мышечная ткань, кровь и т.д.
Особенно много тирозина находится ближе к поверхности клубня.
Ход работы: 1 г сырого картофеля измельчают в ступке с 3 мл дистиллированной воды и быстро фильтруют через марлю.
Фильтрат содержит тирозиназу. Полученную вытяжку делят на две части. Одну часть кипятят. Затем в обе пробирки добавляют по 5-10 капель 0,1% раствора тирозина и помещают их в штатив при комнатной температуре. Пробирки периодически встряхивают, чтобы усилить соприкосновение раствора с кислородом воздуха. Наблюдают изменения, происходящие в пробирках.
Сделайте вывод.
Опыт № 3. Реакция на сукцинатдегидрогеназу.
Реактивы: 1) янтарная кислота (нейтрализованная)
2) метиленовая синь
Исследуемое вещество: мышечная ткань.
Ход работы: 0,3 г. хорошо измельченной мышечной ткани растирают в ступке с двенадцатикратным количеством дистиллированной воды и отфильтровывают через марлю, не отжимая. Экстракцию мышечной ткани повторяют еще раза два. После последней экстракции мышечную кашицу заливают водой и используют полученный раствор с кашицей.
В две пробирки помещают по 3-4 мл р-ра мышечной кашицы. В первую пробирку прибавляют около 0,5 мл нейтрализованного раствора янтарной кислоты. Затем в обе пробирки добавляют по 1 капле метиленовой сини, встряхивают и ставят на водяную баню при 37°С. Через некоторое время наблюдают обесцвечивание раствора в одной из пробирок. В какой?
Фермент сукцикатдегидрогеназа относится к анаэробным дегидрогеназам, классу оксидоредуктаз. Т.е. они участвуют в переносе водорода от окисляемого субстрата - янтарной кислоты - на какой-то промежуточный субстрат, в опыте таким промежуточным субстратом является метиленовая синь. Это фермент, коферментом которого является НАД, содержащий в качестве активного центра витамин РР. Схематично происходящие в пробирке процессы можно изобразить следующим образом:
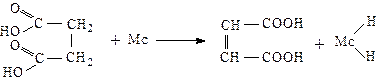
Янтарная кислота фумаровая кислота
Опыт № 4. Определение каталазы.
Общие понятия.
В процессе тканевого дыхания в организме образуется не только Н2О, но и Н2О2, которая является токсичным веществом и для ее устранения организм располагает ферментом, разрушающим перекись водорода на воду и кислород. Это фермент каталаза. Ее много содержится в крови, печени, молоке и в растительных продуктах.
Реактивы: Н2О2 – 3% раствор
Исследуемое вещество: кровь, печень, мышца и т.д.
Ход определения: В пробирку наливаем 1 мл 3% р-ра Н2О2 и добавляем немного растертой печени, мышцу или немного крови.
Что наблюдаете? Сравнение реакции.
Опыт № 5. Обнаружение пероксидазы.
Общие понятия.
Пероксидаза, фермент, который содержится во многих растительных и животных продуктах. Содержится она в доброкачественных тузлуках. Этот фермент катализирует реакции окисления некоторых фенолов и аминов перекисью водорода или органическими перекисями.
Реактивы: 1) р-р бензидина в спирте - 1% (свежеприготовленный)
2) Н2О2 – 3% раствор.
Исслед. в-во: тузлук, мышца рыбы, мясо и т.д.
Ход работы: Приготавливают 4 пробирки, так, как указано в таблице №4 (пр. 1,2,3,4).
Таблица №4
| № проб | Количество вещества каплями | Результат (окраска) | ||||
| бензидин | тузлук | кипяч. тузлук | H2O | H2O2 | ||
| - | - | |||||
| - | - | |||||
| - | - | |||||
| - | - | - |
Что наблюдаете? Дайте объяснение.
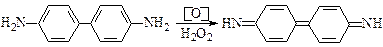
Бесцветное синее
Бензидин неокрашенное соединение. При окислении он превращается в пара-дииминдихинон (п-дииминдихинон) синего цвета.
 2015-05-13
2015-05-13 2003
2003








