Рассмотрим открытую систему, внутри которой установилось равновесие по отношению к температуре и давлению Т,Р=const, т.e в системе отсутствуют такие необратимые процессы, как перенос тепла, вязкие течения. Пусть в ней не достигнуто равновесие к распределению веществ, способных к химическому взаимодействию. Внутри такой системы невозможно возрастание энтропии за счет теплопередачи между ее фазами с различной температурой, и оно обусловлено только химическими реакциями, переносом вещества между фазами и вообще любыми процессами, которые можно охарактеризовать изменениями химических потенциалов. Системы, обладающие такими свойствами находятся в частично равновесном состоянии 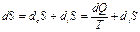 .
.
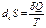 -описывает изменение энтропии открытой системы в результате ее равновесного теплообмена с окружающей средой.
-описывает изменение энтропии открытой системы в результате ее равновесного теплообмена с окружающей средой.
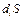 -соответствует самопроизвольному возрастанию энтропии внутри системы за счет химических превращений веществ, находящихся в начальном состоянии.
-соответствует самопроизвольному возрастанию энтропии внутри системы за счет химических превращений веществ, находящихся в начальном состоянии.
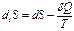
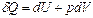 (Работа совершается против сил внешнего давления)
(Работа совершается против сил внешнего давления)
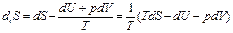
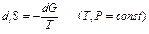
Приращение энтропии открытой системы вследствие внутренних необратимых процессов пропорционально уменьшению ее общего термодинамического потенциала.
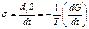
Скорость диссипации свободной энергии задается диссипативной функцией Ф
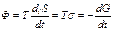
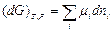
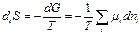
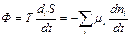
 2015-05-13
2015-05-13 726
726








