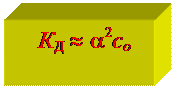 Если a << 1, то
Если a << 1, то
упрощенная формула
закона Оствальда -
a - уменьшается с увеличением концентрации.
Многоосновные слабые кислоты и основания диссоциируют ступенчато:
1 ст.: H2SО3 Û Н+ + HSО3 - К Д1 = 1,7×10-2.
2 ст.: HSО3 - Û H+ + SО32 - К Д2= 6,3×10-8.
раствор имеет сложный ионно-молекулярный состав.
 |
Сильные электролиты диссоциированы полностью:
CaCl2 ® Ca2+ + 2Cl-
Al2(SO4)3 ® 2Al3+ + 3SО42-
Сионов большая Þ свойства зависят от взаимодействия ионов друг с другом и с молекулами Н2О.

 П.Дебай и Э.Хюккель –1923г - ион окружен противоположно заряженными ионами – ионная атмосфера
П.Дебай и Э.Хюккель –1923г - ион окружен противоположно заряженными ионами – ионная атмосфера
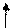
 Чем Сэлектролита Þ среднее расстояние между ионами Þ образование ионных пар.
Чем Сэлектролита Þ среднее расстояние между ионами Þ образование ионных пар.
 |

Ионная сила раствора I -количественная характеристика межионного взаимодействия:
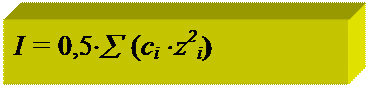
ci – концентрация i -иона
zi - заряд i -иона
g ¹ 1 Þ активность а =g×с.
Для электролита А n В m
 Средний коэффициент активности электролита g ± - среднее геометрическое коэффициентов активности образующих его ионов:
Средний коэффициент активности электролита g ± - среднее геометрическое коэффициентов активности образующих его ионов:
для раствора Аl2(SО4)3 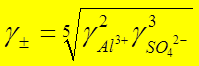
g i - зависят от: 1) природы растворителя и
растворенного вещества;
3) температуры.
| Концентрация моль/1000г H2O | g электролитов | ||||||
| NaCl | KCl | NaOH | KOH | HCl | H2SO4 | CaCl2 | |
| 0,001 0,01 0,1 0,5 1,0 2,0 5,0 | 0,965 0,874 0,778 0,681 0,657 0,668 0,874 | 0,966 0,901 0,769 0,651 0,607 0,576 - | 0,966 0,900 0,776 0,693 0,679 0,700 1,060 | 0,966 0,900 0,766 0,712 0,735 0,683 1,670 | 0,966 0,904 0,796 0,758 0,809 1,010 2,380 | 0,830 0,544 0,265 0,156 0,132 0,128 0,208 | 0,840 0,580 0,518 0,448 0,500 0,792 0,890 |
· в области высококонцентрированных растворов Þ единицы, десятки и даже сотни.
· в области разбавленных растворов Þ к 1
· в области разбавленных растворов (ниже 0,1 моль/л) g зависят от концентрации и заряда ионов и мало зависят от природы растворенных веществ.
 |
| Ионы | Коэффициент активности для ионной силы | |||||
| 0,001 | 0,01 | 0,02 | 0,05 | 0,07 | 0,1 | |
| водорода Однозарядные Двухзарядные Трёхзарядные | 0,98 0,98 0,77 0,73 | 0,92 0,92 0,58 0,47 | 0.90 0,89 0,50 0,37 | 0,88 0,85 0,50 0,37 | 0,86 0,83 0,36 0,25 | 0,84 0,80 0,30 0,21 |
Задача
Определить активность ионов в 0,01 М растворе СаСl2.
СаCl2 ® Ca 2+ + 2Cl-
С моль/л: 0,01 0,012×0,01 моль/л
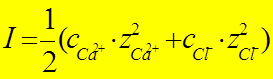 =1/2(0,01×4+0,02×1)= 0,03
=1/2(0,01×4+0,02×1)= 0,03
а = 
Коэффициент активности g находят:
1)по таблице: I = 0,03 Þ 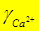 » 0,47;
» 0,47; 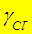 » 0,87.
» 0,87.
а 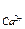 =
= 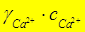 = 0,47×0,01 = 4,7×10-3 (моль/л)
= 0,47×0,01 = 4,7×10-3 (моль/л)
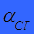 =
= 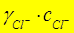 = 0,87×0,02 = 1,74×10-2 (моль/л).
= 0,87×0,02 = 1,74×10-2 (моль/л).
2) по формулам:
 если I £ 0,01
если I £ 0,01
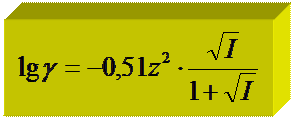
если 0,1 > I > 0,01
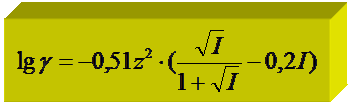 |

если I» 1

Вода - очень слабый электролит:
Н2О + Н2О Û Н3О+ + ОН-
 самоионизация
самоионизация
 молизация
молизация
Н2О Û Н+ + ОН-; D H 0 298дисс = 55,9 кДж
D S 0298 дисс = -80,48 Дж/К
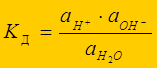 =1,8×10-16 при 25оС
=1,8×10-16 при 25оС
а Н2О = const
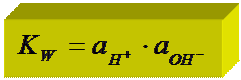
ионное произведение Н2О:
D G0дисс= D Н0дисс - ТD S0дисс =-RTlnKW
lnKW =-55900/8,31×298 - 80,48/8,31×298
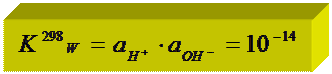
KW = 10-14
K398W = 74×10-14
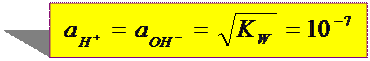
моль/л
ионы Н+ - носители кислотных свойств
ионы ОН- - носители основных свойств.
Прологарифмируем ионное произведение Н2О
lgKW= lgaH+ + lgaOH- = -14
пусть - lgaH+ = рН – водородный показатель
-lgaOH- = рОН - показатель ионов ОН-
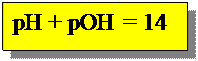 логарифмическая форма ионного произведения Н2О:
логарифмическая форма ионного произведения Н2О:
при 295 К
| среда | СН+, моль/л | СОН-,моль/л | рН |
| Нейтральная | 10-7 | 10-7 | |
| Кислая | >10-7 | <10-7 | <7 |
| щелочная | <10-7 | >10-7 | >7 |

 |
а) для кислот: а Н + » сН+ рН» - lg сН+
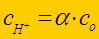 Þ
Þ 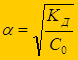 Þ
Þ 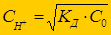 Þ рН = -lg с Н+
Þ рН = -lg с Н+
б) для оснований: а ОН-» сОН- рОН» - lg сОН-
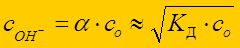 Þ рН = 14 + lgсOH -
Þ рН = 14 + lgсOH -
 |
а) для кислот:
Iр-ра = 0,5× å (сi ××z2i ) Þ gН+ (по таблице или формуле) Þ а Н + = gН+ ×сН+ Þ рН = -lg а Н +
б) для оснований:
Iр-ра = 0,5× å (сi ××z2i ) Þ gOН-(по таблице или формуле) Þ а ОН - = gОН-×сОН- Þ рН = 14 + lg а ОН -
 2015-05-26
2015-05-26 1556
1556








