В разбавленных растворах зависимость коэффициента активности иона от ионной силы описывается уравнением Дебая-Гюккеля:
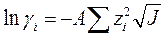 ,
,
где zi – заряд иона.
Если реагируют z A и z B, то z¹ = z A + z B.
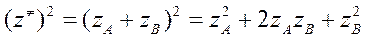 ,
,
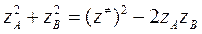 ,
,
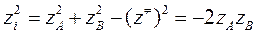 ,
,
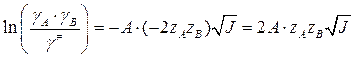 .
.
Это влияние ионной силы называют первичным солевым эффектом.
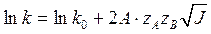
Уравнение Дебая-Гюккеля является приближением и верно лишь для разбавленных растворов. Изменение ионной силы приводит к изменению степени диссоциации слабого электролита.
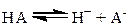 ,
,
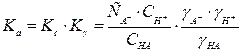 .
.
С ростом ионной силы величины gA и gH убывают, так как Kg падает, Ka = Const. В результате Kc растет и константа скорости реакции увеличивается. Это явление называют вторичным солевым эффектом
 2015-06-14
2015-06-14 579
579







