Соль можно рассматривать как продукт взаимодействия кислоты с основанием. В зависимости от силы электролита получается четыре типа средних солей (см. табл. 2).
Таблица 2
| Тип соли | Сила электролита, образующего соль | Соли | |
| кислота | основание | ||
| I | Сильная | Сильное | NaNO3, KCl, NaJ |
| II | Сильная | Слабое | NH4Cl, CuSO4, Al2(SO4)3, Zn(NO3)2 |
| III | Слабая | Сильное | NaCN, CH3COONa, Na2S, K2CO3 |
| IV | Слабая | Слабое | NH4CN, (NH4)2S, ZnCO3, Al2S3 |
Из приведенных четырех типов солей только II, III, IV подвергаются гидролизу. Гидролиз соли – это взаимодействие ионов соли с ионами воды, приводящее к изменению концентрации последних, в результате чего характер среды может быть (рН < 7, рН > 7, рН» 7). Причиной гидролиза соли является наличие иона слабого электролита в молекуле соли, а результатом – образование слабого электролита. Вот почему гидролизу могут подвергаться соли только II, III, IV типов. Гидролиз – процесс обратимый, зависящий от концентрации соли в растворе и температуры. Повышение температуры и уменьшение концентрации соли увеличивает полноту гидролиза. Количественными характеристиками обратимого процесса гидролиза соли являются константа гидролиза Кг и степень гидролиза h, показывающая, какая часть растворенных молекул подверглась гидролизу.
Пример 9. Доказать, что соль NaNO3 (I тип) гидролизу не подвергается.
Соль NaNO3 образована сильной кислотой и сильным основанием (см. Кд в табл. 1). В водном растворе соль диссоциирует по уравнению
NaNO3 «Na+ + 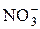 ;
;
вода: H2O «H+ + ОН–. Но ионы Na+ и 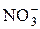 с ионами ОН– и H+ не образуют молекулы NaOH и НNO3, в силу того, что последние являются сильными электролитами и существуют в растворе в виде ионов. Водородный показатель (рН) водных растворов солей I типа равен 7.
с ионами ОН– и H+ не образуют молекулы NaOH и НNO3, в силу того, что последние являются сильными электролитами и существуют в растворе в виде ионов. Водородный показатель (рН) водных растворов солей I типа равен 7.
Пример 10. Гидролиз солей, образованных сильной кислотой и слабым основанием (II тип), например Zn(NO3)2.
В водном растворе Zn(NO3)2 диссоциирует по уравнению:
Zn(NO3)2 «Zn2+ + 2 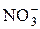 .
.
Из ионов только Zn2+ будет подвергаться гидролизу, так как является ионом слабого основания Zn(OH)2 (см. Кд в табл. 1). Ион Zn2+ – многозарядный, поэтому гидролизуется по ступеням соответственно ступенчатой диссоциации основания. Каждая ступень характеризуется величиной КГ и h. Так, гидролиз Zn(NO3)2 может быть выражен уравнениями:
Первая ступень
Zn2+ + H2O «ZnOH+ + H+, pH < 7;
Zn(NO3)2 + H2O «ZnOHNO3 + HNO3.
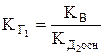 ;
; 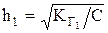 .
.
Вторая ступень
ZnОН+ + H2O «Zn(OH)2 + H+, pH < 7;
ZnОНNO3 + H2O «Zn(OH)2 + HNO3.
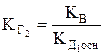 ;
; 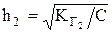 .
.
Соль по первой ступени гидролизуется в бóльшей степени, чем по второй: 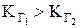 .
. 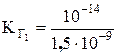 = 6,6×10–6;
= 6,6×10–6; 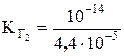 = 2,2×10–10.
= 2,2×10–10.
При обычных условиях вторая ступень гидролиза практически не протекает (ввиду накопления большого количества ионов водорода процесс смещается в сторону образования ZnOH+). Однако разбавление раствора, повышение температуры или связывание ионов водорода приводит к полному гидролизу соли.
Пример 11. Гидролиз солей, образованных слабой кислотой и сильным основанием (III тип), например Na2SO3.
В водном растворе соль Na2SO3 диссоциирует по уравнению:
Na2SO3 «2 Na+ + 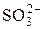 .
.
Ионом слабого электролита – кислоты является 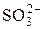 (см. Кд в табл. 1). Сульфит-ион – многозарядный и гидролизуется ступенчато.
(см. Кд в табл. 1). Сульфит-ион – многозарядный и гидролизуется ступенчато.
Первая ступень
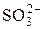 + H2O «
+ H2O «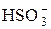 + OH–, pH > 7;
+ OH–, pH > 7;
Na2SO3 + H2O «NaНSO3 + NaOH.
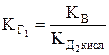 ;
; 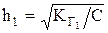 .
.
Вторая ступень
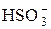 + H2O «H2SO3 + OH–, pH > 7;
+ H2O «H2SO3 + OH–, pH > 7;
NaНSO3 + H2O «H2SO3 + NaOH.
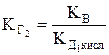 ;
; 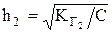 .
.
Соль по первой ступени гидролизуется в бóльшей степени, чем по второй: 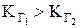 .
. 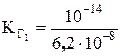 = 1,6×10–7;
= 1,6×10–7; 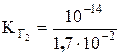 = 5,8×10–13.
= 5,8×10–13.
При обычных условиях вторая ступень гидролиза практически не протекает (ввиду накопления большого количества ионов OH– процесс смещается в сторону образования 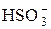 ). Разбавление раствора, повышение температуры или связывание гидроксид-ионов приводит к полному гидролизу соли.
). Разбавление раствора, повышение температуры или связывание гидроксид-ионов приводит к полному гидролизу соли.
Пример 12. Гидролиз солей, образованных слабой кислотой и слабым основанием (IV тип), например NH4NО2.
Соли такого типа даже при обычных условиях гидролизуются до конца.
Диссоциация соли в водном растворе протекает по уравнению:
NH4NО2 «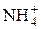 +
+ 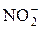 .
.
Оба иона – ионы слабых электролитов NН4OH и НNO2 (см. Кд в табл. 1). Уравнение гидролиза
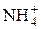 +
+ 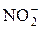 + H2O «NН4OH + НNO2;
+ H2O «NН4OH + НNO2;
NH4NО2 + H2O «NН4OH + НNO2.
При гидролизе солей IV типа рН водных растворов солей может быть меньше семи, если кислота сильнее основания; больше семи, если кислота слабее основания; нейтральной, если сила кислоты и сила основания одинаковы. В результате гидролиза соли NH4NО2 образуется NН4OH (Кд = 1,79×10–5) и НNO2 (Кд = 4,6×10–4). Кислота сильнее основания, следовательно, рН < 7.
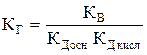 ;
; 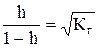
Для соли NH4NО2
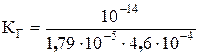 = 1,2×10–6.
= 1,2×10–6.
 2015-06-14
2015-06-14 2115
2115
