В насыщенном растворе малорастворимого электролита произведение концентраций его ионов, возведённых в степень их стехиометрических коэффициентов, есть величина постоянная при данной температуре и называется произведением растворимости (ПР). Так, в насыщенном растворе малорастворимого электролита PbJ2 устанавливается динамическое равновесие:
PbJ2(тв) «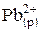 + 2
+ 2 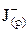 .
.
Количественно это равновесие характеризуется ПР, которое равно произведению концентраций ионов электролита в растворе: 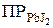 = [Рb2+] [J–]2.
= [Рb2+] [J–]2.
При добавлении к раствору вещества, например KJ, содержащего йодид-ионы, концентрация их увеличивается. Согласно принципу Ле Шателье, происходит смещение равновесия в сторону образования малорастворимого соединения.
Если малорастворимый электролит, записанный в общем виде как AmBn, диссоциирует по уравнению
AmBn «mА+ + nВ–,
то выражение для произведения растворимости будет иметь вид:
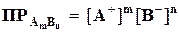 .
.
1. Условие растворения осадка. Произведение концентраций ионов, возведённых в степень стехиометрических коэффициентов, должно быть меньше величины произведения растворимости
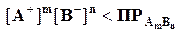 .
.
2. Условие образования осадка. Произведение концентраций ионов, возведённых в степень стехиометрических коэффициентов, должна быть больше величины произведения растворимости
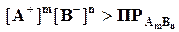 .
.
Величины ПР некоторых соединений приведены в табл. 2 Приложения.
Пример 7. Смешивают равные объёмы 0,01 М растворов AgNО3 и NaCl. Будет ли выпадать осадок AgCl, если ПРАgС1 = 1,6×10-10 (табл. 7)?
Суммарный объём раствора вдвое больше объёма каждого из исходных растворов. Следовательно, после смешивания концентрация ионов Ag+ и Cl– будет вдвое меньше по сравнению с исходной, т.е. [Ag+] = 0,005 = 5×10–3 и
[Сl–] = 0,005 = 5×10–3 моль/л. Находим произведение концентраций Ag+ и Cl– при смешивании: [Ag+] [Сl–] = 2,5×10–5. Так как произведение [Ag+] [Сl–] = 2,5×10–5 больше ПРАgС1 = 1,6×10-10, то осадок выпадает.
4.3. Ионное произведение воды (Кв). Водородный показатель (рН)
Вода, являясь очень слабым электролитом, диссоциирует на ионы:
Н2О «H+ + ОН–; DН0 = 55,835 кДж/моль.
Произведение концентраций ионов H+ и ОН– при данной температуре есть величина постоянная и называется ионным произведением воды (Кв)
Kв = [H+] × [ОН–] = 10–14 пpи 25 °C.
Величина Kв изменяется в зависимости от температуры. Так, при температуре 100 °С Kв = 74×10–14. В водных растворах реакция среды зависит от соотношения концентрации ионов H+ и ОН–. В нейтральной среде [H+] = [ОН–] = 10–7 моль/л; в кислой среде [H+] > [ОН–] при [H+] > 10–7 моль/л: в щелочной среде [H+] < [ОН–] или [H+] < 10–7 моль/л. Вместо концентрации ионов водорода пользуются водородным показателем рН:
рН = –lg[H+].
В нейтральной среде рН = 7, в щелочной среде рН > 7, в кислой среде рН < 7. Для приблизительного определения рН используют разные индикаторы, например, лакмус, фенолфталеин, метиловый оранжевый и др. (см. табл. 3 Приложения).
Пример 8. Вычислите рН 0,0001 н раствора NaOH. Гидроксид натрия полностью диссоциирует на ионы.
Водный раствор NaOH, имеющий концентрацию 0,0001 н содержит гидроксид-ионов 10–4 моль/л; Следовательно, концентрация Н+ будет
[Н+] = Кв/[ОН–] = 10–14/10–4 = 10–10 моль/л.
Отсюда pH = –lg[H+] = –lg[10–10] = 10
 2015-06-14
2015-06-14 809
809








