Леккия №17
РАСТВОРЫ
План
1. Общая характеристика растворов.
2. Способы выражения концентрации растворов.
3. Термодинамика и механизм процесса растворения.
4. Растворимость.
5. Вода как растворитель. Значение растворов в жизнедеятельности организмов
Общая характеристика растворов.
Растворы – это гомогенные системы переменного состава, включающие два и более компонентов. Частицы компонентов раствора распределены по его объему в виде атомов, молекул или ионов (размер частиц 0,1 – 0,5 нм).
Образование растворов, в отличие от механических смесей, сопровождается изменением энтальпии, энтропии и объема системы.
По агрегатному состоянию различают газовые, жидкие и твердые растворы. Но обычно термин растворы относится к жидким системам.
Способы выражения концентрации растворов.
Относительное содержание компонентов в растворе определяется его концентрацией.
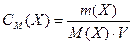 |
Молярная концентрация – это количество вещества, содержащееся в одном литре раствора (моль/л):
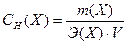 |
Эквивалентная концентрация – это число молей эквивалентов вещества, содержащихся в одном литре раствора (моль/л):
Эквивалент – это реальная или условная частица вещества, которая в кислотно-основной реакции эквивалентна одному иону водорода, а в окислительно-восстановительной эквивалентна одному электрону.
Масса одного моля эквивалентов называется молярной массой эквивалента вещества (Э). В разных реакциях одно и то же вещество может иметь разные эквиваленты.
Моляльная концентрация – это количество вещества, содержащееся в одном килограмме растворителя (моль/кг):
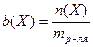 |
Массовая доля равна отношению массы растворенного вещества к массе раствора:
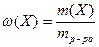 |
Молярная доля равна отношению количества растворенного вещества в общему количеству веществ в растворе:
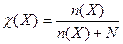 |
Как правило, вещество обладает определенной растворимостью в данном растворителе. Под растворимостью понимают концентрацию вещества в насыщенном растворе.
 2015-06-14
2015-06-14 1003
1003







