Распад растворенного вещества на ионы под действием молекул растворителя называют электролитической диссоциацией или ионизацией вещества в растворах.
Теория электролитической диссоциации была создана в 1884-1887 гг. шведским химиком С. Аррениусом и развита в трудах И.А. Каблукова, В.А. Кистяковского на основе химической (гидратной) теории растворения Д.И. Менделеева. Эта классическая теория позволила объяснить, как электропроводность растворов, так и протекание химических реакций в них.
Основные положения теории электролитической диссоциации:
1. при растворении солей, кислот и оснований в воде происходит ионизация этих веществ с образованием заряженных частиц - ионов: положительных (катионов) и отрицательных (анионов);
2. электрическая проводимость растворов солей, кислот и оснований в воде прямо пропорциональна общей концентрации ионов в растворе.
Возможность и степень распада растворенного вещества на ионы определяется природой растворенного вещества и растворителя. Электролитической ионизации в полярных растворителях подвержены ионные и молекулярные соединения с полярным типом связи. Вода относится к наиболее сильным ионизирующим растворителям (мерой этого воздействия является относительная диэлектрическая проницаемость растворителя, значение которой для воды равно = 84,2). Однако, электролитическую ионизацию в растворе вызывают не только вода, но и неводные полярные растворители, такие как жидкие аммиак, диоксид серы и др.
|
|
|
Электролитическая ионизация обусловлена взаимодействием полярных молекул растворителя с частицами растворенного вещества. Упрощенно, без учета H-связей в воде, этапы электролитической диссоциации представлены на рис.6.2.
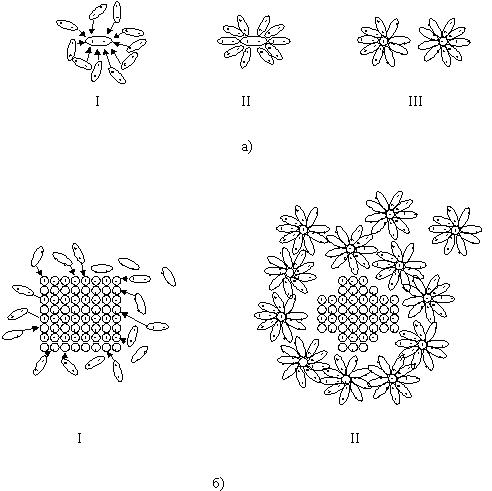
Рис. 6.2. Этапы электролитической ионизации полярных молекул (а) и ионных кристаллов (б):
 2015-06-14
2015-06-14 814
814








