Составьте формулы всех возможных комплексных соединений, используя в качестве комплексообразователя Co3+ (координационное число его равно шести), в качестве лигандов – NH3, NO 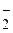 , внешней сферы – K+, NO
, внешней сферы – K+, NO 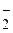 .
.
Решение.
Поскольку координационное число иона кобальта равно 6, во внутренней координационной сфере должно быть 6 лигандов. Заряды внутренней и внешней координационных сфер в сумме равны нулю. Учитывая эти правила, можно составить следующие комплексные ионы и соответствующие им комплексные соединения:
1. [Co(NH3)6]3+, [Co(NH3)6](NO2)3.
2. [Co(NH3)5(NO2)]2+, [Co(NH3)5(NO2)](NO2)2.
3. [Co(NH3)4(NO2)2]+, [Co(NH3)4(NO2)2](NO2).
4. [Co(NH3)3(NO2)3]0, [Co(NH3)3(NO2)3].
5. [Co(NH3)2(NO2)4]–, K[Co(NH3)2(NO2)4].
6. [Co(NH3)(NO2)5]2–, K2[Co(NH3)(NO2)5].
7. [Co(NO2)6]3–, K3[Co(NO2)6].
 2015-06-24
2015-06-24 1835
1835








