1.2.1. Реакции с участием связи O−H
Кислотные свойства. В молекуле спирта содержится атом водорода, связанный с сильно электроотрицательным кислородом, поэтому спирт проявляет заметную кислотность.
Спирты (кроме метанола) более слабые кислоты, чем вода: алкильная группа, проявляя электронодонорный индукционный эффект, подает электроны на кислород R→Оy, увеличивает на нем отрицательный заряд (по сравнению с зарядом на гидроксид-ионе) и делает алкоксид-ион R→Оy - сопряженное основание - более сильным, а кислоту - более слабой.
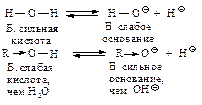
Алкоксиды (алкоголяты) нельзя получить реакцией спирта с гидроксидами металлов, их синтезируют реакцией спирта с активным металлом (Na, K, Mg, Al и др.).
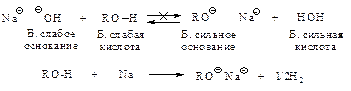
Кислотные свойства спиртов убывают в ряду:
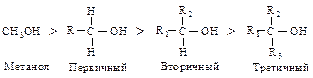
Основность. Спирты представляют собой основания, сравнимые по силе с водой. При действии сильных кислот они превращаются в соли.
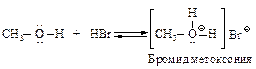
Взаимодействие с магнийгалогеналкилами. В этой реакции происходит замещение гидроксильного водорода на магнийгалоген и выделяется углеводород.
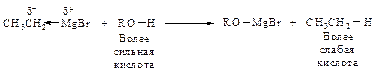
В случае использования СН3MgJ выделяется метан. По объему выделившегося метана определяют количественное содержание гидроксильных групп.
Образование сложных эфиров. Благодаря наличию электронной пары на атоме кислорода спирт является нуклеофильным реагентом. В качестве нуклеофила он выступает в реакциях образования сложных эфиров. Спирт может атаковать электронодефицитный атом углерода карбонильной группы хлорангидридов, ангидридов кислот и кислот (реакция ацилирования спирта).
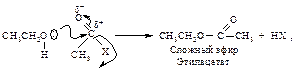
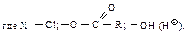
 2015-06-24
2015-06-24 705
705








