Для подробного исследования физико-химических и биологических свойств белков, а также изучения их химического состава и структуры непременным условием является их выделение в химически чистом, гомогенном состоянии. Последовательность операций при этом следующая:
1. измельчение биологического материала (гомогенизация),
2. извлечение протеинов (перевод их в растворенное состояние- экстракция),
3. выделение исследуемого белка из смеси других (очистка и получение индивидуального белка).
Все методы разделения смесей основаны на том, что их компоненты в результате каких-либо манипуляций оказываются в разных участках системы и могут быть механически отделены друг от друга. Очищение индивидуальных белков является ступенчатым процессом, т.к. на первых этапах очистки фракции содержат множество примесей.
Остановимся на наиболее распространённых методах.
1. Ультрацентрифугирование. В его основе лежат различия в молекулярных массах протеинов. В кювету помещают раствор буфера и сверху наносят тонкий слой смеси белков. Сосуд помещают в ультрацентрифугу, при вращении ротора которой создаётся центробежное ускорение, пропорциональное молекулярной массе протеинов. В результате последние оседают в растворе буфера. Причём выпавший осадок расслаивается на отдельные фракции, имеющие разную молекулярную массу (Мr). Их можно легко извлечь. Но этот способ требует много времени и дорогостоящей аппаратуры. Поэтому в последние годы разработаны более простые методы (гель-хроматография и электрофорез).
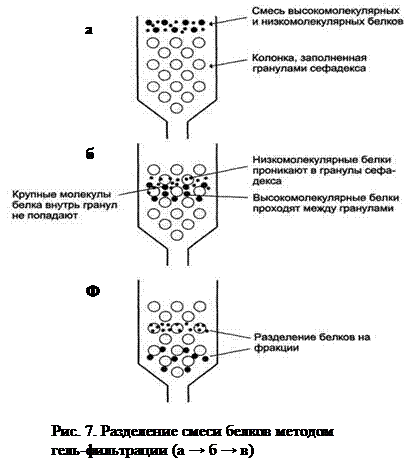
2. Гель-фильтрация (гель-фильтрационная хроматография). Метод основан на том, что вещества, отличающиеся молекулярными массами, по-разному распределяются между подвижной и неподвижной фазами. Хроматографическая колонка (рис. 7) заполняется пористым гелем полисахарида (сефадекса, сефактила, агарозы и др.), представленным в виде гранул с порами. Их размер можно выбирать в зависимости от целей исследования. Внутри гранул находится жидкость, в которую могут проникать низкомолекулярные соединения и белки с небольшой Мr (молекулярной массой). На хроматографическую колонку наносят изучаемую смесь и с помощью подвижной фазы растворителя, вымывают большие мицеллы (белков), а малые, проникая внутрь гранул, задерживаются на некоторое время. Используя диаметр пор оценивают размеры молекул. Легко рассчитать молекулярную массу исследуемого белка, зная объем растворителя.
3.  Электрофорез использует способность протеинов двигаться в электрическом поле со скоростью, пропорциональной их суммарному заряду и обратно пропорциональной их массам. Белки с отрицательным зарядом перемещаются к аноду (+), а с положительным – к катоду (-). Электрофорез проводят на различных носителях: бумаге, крахмальном или полиакриламидном (ПААГ) гелях и т.д. Для обнаружения локализации полимеров носители обрабатывают красителем (бромфеноловым синим или амидовым чёрным), что позволяет обнаружить пятна окрашенных белков.
Электрофорез использует способность протеинов двигаться в электрическом поле со скоростью, пропорциональной их суммарному заряду и обратно пропорциональной их массам. Белки с отрицательным зарядом перемещаются к аноду (+), а с положительным – к катоду (-). Электрофорез проводят на различных носителях: бумаге, крахмальном или полиакриламидном (ПААГ) гелях и т.д. Для обнаружения локализации полимеров носители обрабатывают красителем (бромфеноловым синим или амидовым чёрным), что позволяет обнаружить пятна окрашенных белков.
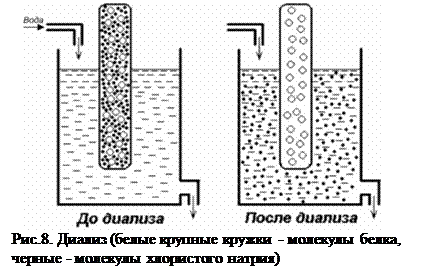
4. Диализ применяют для отделения низкомолекулярных примесей или замены состава среды. Метод основан на том, что молекулы белка из-за своих больших размеров не могут проходить через полупроницаемые мембраны, в то время как вода и низкомолекулярные вещества равномерно распределяются между объемом, ограниченным мембраной, и окружающим раствором (рис. 8). В лаборатории подлежащую диализу смесь помещают в мешок из целлофана и погружают последний в буферный раствор. Непрерывный ток воды через сосуд приводит к полному выходу содержащихся в целлофане низкомолекулярных веществ, а белки остаются внутри.
 2015-06-26
2015-06-26 933
933








