Раздел 1. Теоретические основы аналитической химии
Количественный состав раствора. Количественный состав раствора можно описывать с помощью безразмерных величин и величин, имеющих размерность. Безразмерные величины называются долями. Доля растворенного вещества в растворе может быть массовая (ω), объемная (φ), молярная (χ). Из всех видов долей чаще всего, по крайней мере в аналитической химии, используется массовая доля. Доли могут выражаться в процентах. Процент – это не единица, а всего лишь синоним величины «одна сотая».
Массовая доля – это, согласно современному подходу, не концентрация и называть ее «процентной концентрацией» не следует. Слово «концентрация» переводится на русский язык как «сосредоточение» и относится к растворенному веществу, а не к раствору, т.е. говорят «концентрация растворенного вещества в растворе», а не «концентрация раствора».
К размерным величинам, используемым для описания количественного состава растворов, относят концентрации вещества в растворе и моляльность растворенного вещества.
|
|
|
Концентрация – это отношение массы или количества растворенного вещества к объему раствора. Концентрация растворенного вещества в растворе может быть
массовая – отношение массы растворенного вещества к объему раствора: 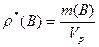 . Массовая концентрация, имеющая размерность г/мл, называется титром раствора;
. Массовая концентрация, имеющая размерность г/мл, называется титром раствора;
молярная (С) – отношение количества растворенного вещества к объему раствора. Понятие «молярная концентрация» может относиться как к формульной единице вещества, так и к его эквиваленту. Молярную концентрацию выражают в моль·дм–3 (моль/л). Например,
С(HCI)=0,1 моль·дм–3 или c (HCI) = 0,1 М;
С(1/5 KMnO4 ) = 0,05 моль·дм–3 или 0,05 М (1/5 KMnO4).
Моляльность растворенного вещества – отношение количества растворенного вещества к массе растворителя. Обозначают моляльность как m(B), b(B), Cm(B). Размерность моляльности – моль/кг. Ее используют в тех случаях, когда раствор находится в неизотермических условиях.
 2015-07-21
2015-07-21 757
757







