Не существует процесса, единственным результатом которого является передача количества теплоты от менее нагретого тела к более нагретому. (Невозможен круговой процесс, единственным результатом которого было бы производство работы за счет охлаждения теплового резервуара)
ΔS = Q/T или Q=TΔ S (или dQ=TdS)
Объединенный 1-ыйи 2-ой закон термодинамики:
ΔU= TΔS–pΔV+A
(dU= TdS–pdV+dA)
A= ΔU +pΔV–TΔS= ΔG
В эти уравнения входят и члены, относящиеся к первому закону термодинамики (работа в форме D G и D F), и описываемая вторым законом функция энтропия (D S).
Основные положения тепловой теоремы (III з-на термодинамики)т заключаются в следующем:
1. При абсолютном нуле температуры свободная энергия X равна теплоте процесса.
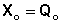 (I.59)
(I.59)
2. При температурах, близких к абсолютному нулю, теплоемкость системы равна нулю.
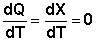 (I.60)
(I.60)
Одной из формулировок третьего начала термодинамики является также постулат Планка:
Энтропия идеального кристалла при абсолютном нуле температуры равна нулю.
 2015-08-12
2015-08-12 340
340








