Бензольное ядро обладает высокой прочностью, чем и объясняется склонность ароматических углеводородов к реакциям замещения. В отличие от алканов, которые также склонны к реакциям замещения, ароматические углеводороды характеризуются большой подвижностью атомов водорода в ядре, поэтому реакции галогенирования, нитрования, сульфирования и др. протекают в значительно более мягких условиях, чем у алканов.
Электрофильное замещение в бензоле
Несмотря на то, что бензол по составу является ненасыщенным соединением, для него не характерны реакции присоединения. Типичными реакциями бензольного кольца являются реакции замещения атомов водорода – точнее говоря, реакции электрофильного замещения.
Рассмотрим примеры наиболее характерных реакций этого типа.
1) Галогенирование. При взаимодействии бензола с галогеном (в данном случае с хлором) атом водорода ядра замещается галогеном.

+ Cl2 –AlCl3®
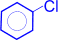
(хлорбензол) + H2O
Реакции галогенирования осуществляются в присутствии катализатора, в качестве которого чаще всего используют хлориды алюминия или железа.
2) Нитрование. При действии на бензол нитрующей смеси атом водорода замещается нитрогруппой (нитрующая смесь – это смесь концентрированных азотной и серной кислот в соотношении 1:2 соответственно).

+ HNO3 –H2SO4®

(нитробензол) + H2O
Серная кислота в данной реакции играет роль катализатора и водоотнимающего средства.
3) Сульфирование. Реакция сульфирования осуществляется концентрированной серной кислотой или олеумом (олеум – это раствор серного ангидрида в безводной серной кислоте). В процессе реакции водородный атом замещается сульфогруппой, приводя к моносульфокислоте.

+ H2SO4 –SO3®

(бензолсульфокислота) + H2O
4) Алкилирование (реакция Фриделя-Крафтса). При действии на бензол алкилгалогенидов в присутствии катализатора (хлористого алюминия) осуществляется замещение алкилом атома водорода бензольного ядра.

+ R–Cl –AlCl3®

(R-углеводородный радикал) + HCl
Следует отметить, что реакция алкилирования представляет собой общий способ получения гомологов бензола - алкилбензолов.
Рассмотрим механизм реакции электрофильного замещения в ряду бензола на примере реакции хлорирования.
Первичной стадией является генерирование электрофильной частицы. Она образуется в результате гетеролитического расщепления ковалентной связи в молекуле галогена под действием катализатора и представляет собой хлорид-катион.
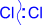 | + AlCl3 ® Cl+ + AlCl4- |
Образующаяся электрофильная частица атакует бензольное ядро, приводя к быстрому образованию нестойкого p- комплекса, в котором электрофильная частица притягивается к электронному облаку бензольного кольца.
 | + Cl+ ® |  | Cl+ |
| · - комплекс |
Иными словами, p- комплекс – это простое электростатическое взаимодействие электрофила и p- электронного облака ароматического ядра.
Далее происходит переход p- комплекса в s- комплекс, образование которого является наиболее важной стадией реакции. Электрофильная частица "захватывает" два электрона s- электронного секстета и образует s- связь с одним из атомов углерода бензольного кольца.
 | Cl+ ® | 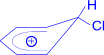 · - комплекс · - комплекс |
· - Комплекс – это катион, лишенный ароматической структуры, с четырьмя p- электронами, делокализованными (иначе говоря, распределенными) в сфере воздействия ядер пяти углеродных атомов. Шестой атом углерода меняет гибридное состояние своей электронной оболочки от sp2- до sp3-, выходит из плоскости кольца и приобретает тетраэдрическую симметрию. Оба заместителя – атомы водорода и хлора располагаются в плоскости, перпендикулярной к плоскости кольца.
На заключительной стадии реакции происходит отщепление протона от s- комплекса и ароматическая система восстанавливается, поскольку недостающая до ароматического секстета пара электронов возвращается в бензольное ядро.

®

+ H+
Отщепляющийся протон связывается с анионом четыреххлористого алюминия с образованием хлористого водорода и регенерацией хлорида алюминия.
H+ + AlCl4- ® HCl + AlCl3
Именно благодаря такой регенерации хлорида алюминия для начала реакции неоходимо очень небольшое (каталитическое) его количество.
Несмотря на склонность бензола к реакциям замещения, он в жестких условиях вступает и в реакции присоединения.
1) Гидрирование. Присоединение водорода осуществляется только в присутствии катализаторов и при повышенной температуре. Бензол гидрируется с образованием циклогексана, а производные бензола дают производные циклогексана.

+ 3H2 –t°,p,Ni®

(циклогексан)
2) На солнечном свету под воздействием ультрафиолетового излучения бензол присоединяет хлор и бром с образованием гексагалогенидов, которые при нагревании теряют три молекулы галогеноводорода и приводят к тригалогенбензолам.
 | + 3Cl2 –hn® | 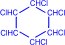 гексахлорциклогексан гексахлорциклогексан | 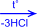 | 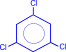 сим-трихлорбензол сим-трихлорбензол |
3) Окисление. Бензольное ядро более устойчиво к окислению, чем алканы. Даже перманганат калия, азотная кислота, пероксид водорода в обычных условиях на бензол не действуют. При действии же окислителей на гомологи бензола ближайший к ядру атом углерода боковой цепи окисляется до карбоксильной группы и дает ароматическую кислоту.
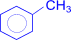
+ 2KMnO4 ®
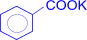
(калиевая соль бензойной кислоты) + 2MnO2 + KOH + H2O
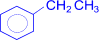
+ 4KMnO4 ®

+ K2CO3 + 4MnO2 + 2H2O + KOH
Во всех случаях, как видно, независимо от длины боковой цепи образуется бензойная кислота.
При наличии в бензольном кольце нескольких заместителей можно окислить последовательно все имеющиеся цепи. Эта реакция применяется для установления строения ароматических углеводородов.
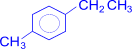
–[O]®
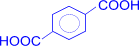
(терефталевая кислота)
Правила ориентации в бензольном ядре
Как и собственно бензол, гомологи бензола также вступают в реакцию электрофильного замещения. Однако, существенной особенностью этих реакций является то, что новые заместители вступают в бензольное кольцо в определенные положения по отношению к уже имеющимся заместителям. Иными словами, каждый заместитель бензольного ядра обладает определенным направляющим (или ориентирующим) действием. Закономерности, определяющие направление реакций замещения в бензольном ядре, называются правилами ориентации.
Все заместители по характеру своего ориентирующего действия делятся на две группы.
Заместители первого рода (или орто-пара-ориентанты) – это атомы или группы атомов, способные отдавать электроны (электронодонорные). К ним относятся углеводородные радикалы, группы –OH и –NH2, а также галогены. Перечисленные заместители (кроме галогенов) увеличивают активность бензольного ядра. Заместители первого рода ориентируют новый заместитель преимущественно в орто- и пара-положение.
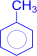
+ 2H2SO4 ®
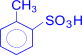
(о-толуолсульфок-та) +
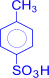
(п-толуолсульфок-та) + 2H2O

+ 2Cl2 –AlCl3®

(о-хлортолуол) +
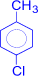
(п-хлортолуол) + 2HCl
Рассматривая последнюю реакцию, необходимо отметить, что в отсутствии катализаторов на свету или при нагревании (т.е. в тех же условиях, что и у алканов) галоген можно ввести в боковую цепь. Механизм реакции замещения в этом случае радикальный.

+ Cl2 –hn®
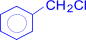
(хлористый бензил) + HCl
Заместители второго рода (мета-ориентанты) – это способные оттягивать, принимать электроны от бензольного ядра электроноакцепторные группировки. К ним относятся:
–NO2, –COOH, –CHO, –COR, –SO3H.
Заместители второго рода уменьшают активность бензольного ядра, они направляют новый заместитель в мета-положение.

+ HNO3 –H2SO4®
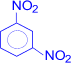
(м-динитробензол) + H2O
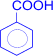
+ HNO3 –H2SO4®
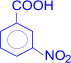
(м-нитробензойная кислота) + H2O
Применение
Ароматические углеводороды являются важным сырьем для производства различных синтетических материалов, красителей, физиологически активных веществ. Так, бензол – продукт для получения красителей, медикаментов, средств защиты растений и др. Толуол используется как сырье в производстве взрывчатых веществ, фармацевтических препаратов, а также в качестве растворителя. Винилбензол (стирол) применяется для получения полимерного материала – полистирола.
 2015-08-21
2015-08-21 2083
2083








