Достоинство атомно–абсорбционного метода, прежде всего, заключается в гораздо более высокой стабильности аналитическогосигнала.
Аналитический сигнал в данном случае – это доля прошедшего света. Он логарифмически связан с концентрацией, поэтому можно осуществить количественный анализ. Обычно он выполняется методом градуировочного графика, который строится непосредственно перед анализом или сразу после анализа раствора с неизвестной концентрацией.
Однако, в силу того, что аналитико-активная форма в атомно-абсорбционном методе – это атомы в пламени, а в атомно-эмиссионном – атомы возбужденные в пламени, то это накладывает существенный отпечаток на погрешность определения.
Атомно-абсорбционный метод позволяет определить вещества с точностью 1-3%, а атомно-эмиссионный метод - 3-5% (относительных). Это обусловлено тем, что аналитико-активная форма в атомно-абсорбционном методе атомы, и концентрация меньше зависят от температуры пламени, от соотношения горячий газ – окислитель, а зависит лишь от скорости подачи в пламя анализируемого раствора. Поэтому градуировочные графики атомно-абсорбционного анализа довольно стабильны и могут служить для работы в течение длительного времени:
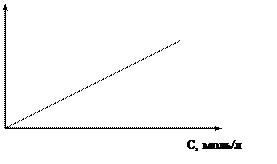 А
А
Рис. 0-7. Градуировочный график атомно-абсорбционного анализа
Очень часто выбор варианта определения зависит от чувствительности метода к тем или атомам.
Метод атомно-абсорбционной спектроскопии позволяет определять почти все металлы. Однако при сравнении чувствительности обоих методов определяемые элементы можно подразделить на три группы:
1) элементы, определяемые с большей чувствительностью методом эмиссионной спектроскопии;
2) элементы, определяемые с большей чувствительностью методом абсорбционной спектроскопии;
3) оба метода дают сопоставимые результаты.
Ниже приведены фрагменты таблицы, взятые у Фрица и Шенка,
позволяющие сравнить пределы обнаружения металлов (мг/мл)
атомно-эмиссионным (АЭ) и атомно-абсорбционным (АА) методами:
Таблица.
Пределы обнаружения металлов (мг/мл) атомно-эмиссионным (АЭ)
и атомно-абсорбционным (АА) методами
| Металл | АЭ | АА | металл | АЭ | АА | Металл | АЭ | АА |
| Li | 3 10-6 | 5 10-3 | Ag | 2 10-2 | 5 10-3 | As | 5 10-1 | |
| Sr | 2 10-4 | 1 10-2 | Co | 3 10-2 | 7 10-3 | Au | 5 10-1 | 1 10-2 |
| Tl | 2 10-3 | 2 10-1 | Cr | 5 10-3 | 5 10-3 | Hg | 2 10-1 | |
| W | 5 10-1 | Cu | 1 10-2 | 5 10-3 | Mg | 4 10-3 | 3 10-4 | |
| Ba | 2 10-3 | 1 10-1 | Nd | Os | ||||
| Eu | 3 10-3 | 2 10-1 | Pr | Si | 5 10-1 | 1 10-1 | ||
| Pd | 5 10-2 | 5 10-1 | Ti | 2 10-1 | 1 10-1 | Sb | 1.5 | 2 10-1 |
| Sc | 3 10-2 | 2 10-1 | U | Zn | 2 10-3 |
В первой части таблицы помещены пределы обнаружения элементов, для которых эмиссионный вариант чувствительнее абсорбционного (это мг/л – или частица на миллион). В эмиссионном варианте лучше определять литий, стронций, теллур, ванадий, вольфрам, европий, палладий, скандий и еще» 15-20 элементов.
Во второй части таблицы приведены пределы обнаружения элементов, для которых эмиссионный и абсорбционный варианты дают сравнимые результаты это – серебро, кобальт, медь, натрий.
Третья часть таблицы – это элементы, где доминирует абсорбционный вариант. Особенно ярко это видно на примере цинка. Понятно, что данная таблица относительна. Почему? Потому что эта таблица дана для пламени динитрооксид-ацетилен. В низкотемпературном пламени ситуация может поменяться.
Недостатком атомно-абсорбционной спектроскопии является дороговизна приборов, их дорогое обслуживание, дорогостоящие материалы.
Методом ААС можно определить 69 элементов, но для этого нужно 69 ламп.
Рассмотрим следующие разновидности атомно-абсорбционногоанализа.
В последнее время широко распространен метод холодного пара. Суть метода в том, что поглощающая среда формируется не в пламени, не в плазме, а при обычной температуре в газовой фазе. Имеется один элемент, который легко получается в газовой фазе в чистом виде, а для ряда элементов получается легко летучие соединения, которые легко обеспечивают значительные концентрации атома в газовой фазе.
Какой это элемент? Конечно, ртуть. Метод основан на том, что ртуть восстанавливается подходящим восстановителем, чаще всего SnCl2 и выдувается азотом из анализируемого раствора в длинную поглощающую кювету (обычная трубка). Далее через эту трубку пропускается узкий луч света ЛПК (лампы с полым катодом) и измеряется его поглощение. Иногда кювета замкнутая, то есть ртуть из анализируемого раствора не выдувается, а все время циркулирует между газовой фазой и анализируемым раствором, то есть создается непрерывный поток. В этом случае сохраняется пропорциональность между концентрацией ртути в растворе и поглощением.
Естественно, при этом поглощение дает информацию о концентрации ртути. Надо отметить, что этот метод уникален по своей чувствительности, так как позволяет определять ртуть на уровне 0,1 ПДК для питьевой воды, а ПДК на ртуть находится на уровне 0,2 ППБ (частиц на миллиард). Естественно, что определение ртути с такой точностью важно с точки зрения охраны окружающей среды.
Теперь можно сравнить, что дает абсорбционный вариант в пламени: 0,2 ППМ. А метод холодного пара – ПДК в 1000 раз более низкое, чем этот предел обнаружения - 0,02 ППД.
Кроме этого, методом холодного пара определяют иногда и другие элементы, так как нет других, более удобных методов определения мышьяка, селена, сурьмы.
Как Вы думаете, в каком виде? Конечно в виде гидридов, так как гидриды их летучие. Правда, параметры чувствительности их гораздо хуже, так как здесь нет атомов, а есть молекулы. Но, тем не менее, этот метод определения мышьяка является одним из лучших.
Вторая разновидность - это электротермический метод анализа или атомно-абсорбционный метод анализа с электротермической атомизацией. Вначале этот метод осуществлялся в электрической дуге, то есть атомизация определяемого вещества шла в электрической дуге. Через дугу пропускался луч света, и таким образом получался аналитический сигнал.
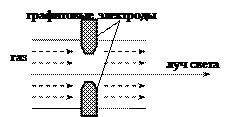 |
Рис. 0-8.
Но эта система была нестабильна, и поэтому об этом методе серьезно не говорили. Революция произошла в конце 60-х годов, когда была предложена графитовая кювета или платформа Львова, профессора технологического института Санкт-Петербурга, удостоенного медали спектрального общества за свою уникальную разработку.
Платформа Львова выглядит следующим образом: это графитовая трубка длиной 2 см, по центру которой имеется отверстие 2 мм. В это отверстие автоматической микропипеткой вносят до 10 мкл анализируемого раствора. Стенки ее могут быть покрыты тугоплавкими металлами или окислами.
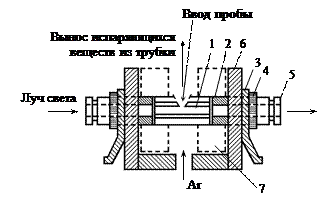
1 - графитовая трубка, кювета;
2 - графитовые шайбы для контакта;
3 - контакт для кабеля от блока питания;
4 - гайки;
5 - патрубки, снабженные кварцевыми окнами;
6 - стойки;
7 - цилиндры, охлаждаемые водой.
Рис 0-9. Кювета Львова
Кювета эта помещается в устройство с двумя полуэлектродами, которые плотно прижимаются к ней. После того, как проба введена в кювету (большая капля 50 мкл), на два электрода подают мощный ток.
Поскольку графит проводит ток и при этом нагревается до высокой температуры, это обеспечивает атомизацию. Надо отметить, что поднятие температуры во времени происходит скачкообразно, в начале медленно, а потом резко. На рисунке приведен график поднятия температуры. Все это делается автоматически, имеется автоматическая приставка, которая подает напряжение во времени.
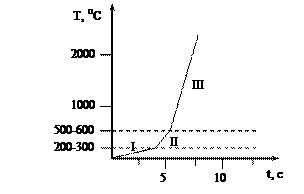 |
Рис.0-10. Изменение температуры кюветы во времени
Вначале, в течение довольно большого промежутка времени, температура медленно поднимается до 200-300°С, при этом происходит испарение растворителя анализируемой пробы и получение твердых форм вещества, кристаллов, кристаллогидратов. Медленно нарастает температура, для того чтобы капля не разбрызгалась и осталась в той точке, куда ее ввели.
На втором этапе температура поднимается более резко, до 500-600°С. При этом происходит разрушение кристаллогидратов без взрыва и разрушение легко разлагающихся солей аммония, карбонатов и некоторых других.
На третьем этапе температура поднимается достаточно резко, почти скачкообразно, до 2000°С, иногда 3000°С. На третьем этапе автоматически включается лампа с полым катодом и начинается регистрация аналитического сигнала – абсорбции. В данном случае максимальный аналитический сигнал (max пика абсорбции) отмечается при температуре 2000°С, т.е. при достижении температуры атомизации на третьем участке. При этом атомы испаряются и атомизируются. Возникает вопрос, почему образуется пик?
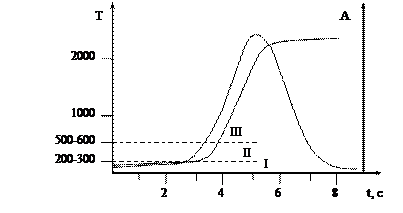 Дело в том, что при высоких температурах атомы определяемого металла и др. соединений, которые есть в пробе, очень быстро разлетаются, разбегаются в стороны и осаждаются на холодных стенках графитовой кюветы, и концентрация быстро падает.
Дело в том, что при высоких температурах атомы определяемого металла и др. соединений, которые есть в пробе, очень быстро разлетаются, разбегаются в стороны и осаждаются на холодных стенках графитовой кюветы, и концентрация быстро падает.
Рис. 0-11. Изменение температуры кюветы
и интенсивности излучения от времени
Только в короткий промежуток времени достигается максимум концентрации атомов и поглощения. Суть метода заключается в том, что при температуре 3000°С наблюдается испарение и атомизация определенного элемента, и включается лампа с полым катодом.
Величина А измеряется в какой - либо момент времени после начала процесса, например, в момент максимума А. Сначала строят калибровочный график зависимости. Затем определяют атомное поглощение для анализируемого объекта и по калибровочному графику находят концентрацию.
При анализе проба быстро охлаждается на стенках кюветы. Далее пробу продувают азотом или аргоном, чтобы удалить содержимое из кюветы и использовать кювету вторично.
Аналитический сигнал обрабатывают ЭВМ, и по высоте пика, либо по его площади находят концентрацию.
Основное достоинство метода атомно-абсорбционного анализа с электротермической атомизацией заключатся в повышении чувствительности прибора в 100 раз, но при этом точность анализа резко падает. Мы говорим не о концентрациях, а о величинах рС + 0,2-0,3 (+ 100-50%). С таким диапазоном можно проводить определение. Но зато этот вариант атомно-абсорбционного анализа позволяет измерять не единицы ППМ (это обычная чувствительность атомно-абсорбционного анализа), а доходить до уровня «десяток».
Этот метод применим в области экологии для контроля вод, почв (анализ микроэлементов в почве), для анализа продуктов питания (токсиканты в молоке и мясе). Для большинства элементов этот метод позволяет достигать уровня ПДК, и даже опускаться ниже.
Например, ПДК по меди в питьевой воде находится на уровне 0,01-0,02 мг/л. Чувствительность пламенного варианта - 1мг/л, а чувствительность непламенного варианта 0,01-0,005 мг/л, т. е. содержание меди в воде явно попадает в область ПДК.
 2015-08-21
2015-08-21 4748
4748







