Запишем уравнение реакции между фотоном и нейтральным атомом натрия.
Полная запись с участием фотонов приобретает вид:
Na0 + hv1 = Na+ + e-. (4.4)
Сделанная запись показывает, что атом натрия (свободный) не может сам отдать электрон и превратиться в ион натрия, так как отрыв электрона требует выполнения "работы выхода", которая и совершается под действием фотона с частотой v1. Нижний индекс - 1 - характеризует частоту, которая необходима для отрыва электрона.
Эта частота - является важнейшей КОНСТАНТОЙ для всей фотохимии, так как ее физический смысл, имеющий теоретическое обоснование только для спектра водорода, носит название константы Ридберга. Теоретического подхода к вычислению аналогичной величины для самых разнообразных атомов и молекул НЕ СУЩЕСТВУЕТ. Сами же эти величины легко определяются экспериментально, а наличие таблиц этих величин КВАНТОВОЙ ХИМИИ позволит надеяться на создание адекватной теории.
Желая указать связь этой константы с константой Ридберга, мы будем называть ее "Ридс", где буква "с", написанная через черточку, означает "специфичность" этой константы, определяемой из условий реакции.
13. Константы фотохимического равновесия
Запишем константу фотохимического равновесия для первой стадии химического процесса:
Kфотохим1 = 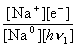 = Kфх1. (4.5)
= Kфх1. (4.5)
Запись справа является сокращением записи константы слева, так как левая требует слишком много букв. Но это не значит, что у новых констант фотохимического равновесия не было отличия от традиционной записи.
Запишем уравнение реакции между свободным электроном и нейтральным атомом хлора. Полная запись с участием фотонов приобретает вид:
Cl0 + e- = Cl- + hv2. (4.6)
Здесь захват электрона нейтральным атомом хлора связан с выделением "энергии сродства к электрону", которая высвечивается в виде фотона с частотой v2.
Запишем константу фотохимического равновесия для этой стадии химического процесса:
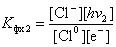 .
.
Последняя стадия этого химического процесса состоит в образовании связи между ионами натрия и хлора, а энергия образовавшейся связи выделяется в виде фотона с частотой v3:
Na+ + Cl- = NaCl + hv3. (4.7)
Запишем константу фотохимического равновесия и для этой стадии химического процесса:
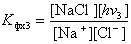 . (4.8)
. (4.8)
Последняя константа фотохимического равновесия отличается от обычной константы, принятой в химии тем, что в знаменателе стоят ионы, а не свободные атомы натрия и хлора. Но, пользуясь выражениями (4.4) и (4.6), можно совершить замену. Используя формулу (4.5) находим выражение для иона натрия, фигурирующего в формуле (4.8):
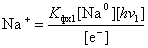 . (4.9)
. (4.9)
Подобным образом находим:
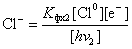 . (4.10)
. (4.10)
Нетрудно видеть, что сокращая концентрацию электронов, получим:
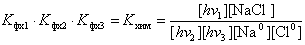 . (4.11)
. (4.11)
Полученный результат показывает, что полное выражение урезанной константы химического равновесия, игнорирует излучение, которое используется в химическом процессе.
Но до сих пор эта урезанная запись не приводила к особым недоразумениям. Это так и будет, если излучение соответствует формуле Планка, дающей распределение излучения в спектре абсолютно черного тела.
Если же, под действием внешних источников, плотность излучения отличается от того, что следует из формулы Планка, то мы и обнаруживаем несостоятельность обычной константы. Эта возможность и используется при подаче резонансного излучения в сферу реакции.
14. Тепловой эффект химической реакции
Мы еще не выразили тепловой эффект химической реакции Q через участников реакции при полном описании. Нетрудно видеть, что тепловой эффект химической реакции легко выражается через фотоны. Алгебраическая сумма поглощенных и излученных фотонов дает выражение для теплового эффекта реакции.
 2015-10-16
2015-10-16 453
453








