| Разложение при прокаливании |  |
| Cоль+металл |  |
| Соль+соль |  |
| Соль+щелочь |  |
| Соль+кислота |  |
При неполном замещении ионов водорода в молекуле кислоты на ионы металлаобразуются кислые соли (гидросоли).
Это наблюдается при взаимодействии многоосновной кислоты с основаниями в тех случаях, когда количество взятого основания недостаточно для образования средней соли. Общая формула: Mex(HzЭOy)n.
 ,
,
 .
.
При частичном замещении гидроксид-ионов в молекуле основания кислотным остаткомобразуются основные соли (гидроксосоли).
Основные соли могут быть образованы только многокислотными основаниями в тех случаях, когда взятого количества кислоты недостаточно для получения средней соли. Общая формула: (MeOH)x(ЭOy)n.
 ,
,
 .
.
Двойные соли состоят из ионов двух разных металлов и кислотного остатка. Например,  ,
,  – калий натрий карбонат.
– калий натрий карбонат.
Смешанные соли – содержат один ион металла и анионы двух кислот  – алюминий хлорид сульфат.
– алюминий хлорид сульфат.
В состав комплексных солей входят сложные (комплексные) ионы (в формулах они заключаются в квадратные скобки). Пример: 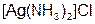 ,
,  .
.
Между классами неорганических соединений существует тесная генетическая связь.
 2015-10-22
2015-10-22 933
933







