Диаграммы состояния бинарных систем.
Закон Рауля. Диаграммы «давление - состав»,
«температура - состав» для неограниченно смешивающихся жидкостей. Первый закон Коновалова. Фракционная перегонка неограниченно смешивающихся жидкостей. Азеотропные смеси.
Второй закон Коновалова.
Фазовое равновесие раствор-пар растворителя (закон Рауля)
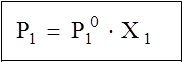 Испарение зависит от температуры и площади поверхности растворителя. В растворах часть поверхности занята молекулами растворенного вещества, что препятствует испарению молекул растворителя. Кроме того, растворенные молекулы способны удерживать вокруг себя молекулы растворителя (процесс сольватации или гидратации) и не дают им испаряться. Все это приводит к тому, что давление пара над раствором оказывается меньше, чем над чистым растворителем (закон Рауля)
Испарение зависит от температуры и площади поверхности растворителя. В растворах часть поверхности занята молекулами растворенного вещества, что препятствует испарению молекул растворителя. Кроме того, растворенные молекулы способны удерживать вокруг себя молекулы растворителя (процесс сольватации или гидратации) и не дают им испаряться. Все это приводит к тому, что давление пара над раствором оказывается меньше, чем над чистым растворителем (закон Рауля)
(1)
где Р10 – давление пара над чистым растворителем.
Формулировка закона Рауля: давление пара над раствором какого-либо компонента пропорционально молярной доле этого компонента в растворе.
Закон Рауля можно сформулировать и через молярную долю растворенного вещества: относительное понижение давления пара над раствором по сравнению с чистым растворителем равно молярной доле растворенного вещества.
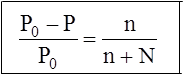 Р0 – давление пара чистого растворителя (2) Р – давление пара раствора
Р0 – давление пара чистого растворителя (2) Р – давление пара раствора
n – число молей растворенного вещества
N – число молей растворителя
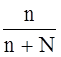 - молярная доля растворенного вещества
- молярная доля растворенного вещества
Понижение давления пара растворителя над раствором влияет на температуру кипения и замерзание раствора. При температуре кипения давление пара над жидкостью должно быть равно внешнему давлению, а при температуре замерзания – давлению пара над затвердевшей жидкостью. Снижение давления пара приводит к необходимости нагревать раствор до более высокой температуры, чтобы достигнуть давления, при котором закипает чистая жидкость, и наоборот, охлаждать до более низкой температуры.
 2020-04-12
2020-04-12 247
247







