Тема урока «Ионная химическая связь»
Цель урока: формирование знаний о природе Восточной
Сибири, особенностях её равнинных территорий.
Задачи урока:
Образовательные: выявить факторы, влияющие на компоненты
природы этого крупного района.
Развивающие: развивать умение самостоятельно работать с
различными источниками географических знаний, создавать
образ территории, развивать речь, географическое мышление,
способности к самостоятельному решению учебных задач,
коммуникативные качества.
Воспитательные: воспитывать любовь и бережное отношение к
природе России и её богатствам.
Цель: изучить механизм образования ионной химической связи.
Задачи:
Образовательные:
- Повторить, скорректировать и закрепить знания по теме «Строение атомов»;
- Ввести понятия «ионы», «ионная связь»;
- Изучить новый тип химической связи – ионную связь, ее природу и условия образования;
- Обучить навыкам сравнения схем строения нейтральных атомов и ионов.
Развивающие:
- Закрепить знания учащихся о распределении электронов в атоме;
- Закрепить понятия о металлах и неметаллах;
- Формировать умения определять вид ионной химической связи.
Воспитательные:
|
|
|
Ресурсы урока:
1. Учебник: Химия. 8 класс. Базовый уровень: учеб. Для общеобразоват. учреждений / О.С. Габриелян
2. Таблица Д. И. Менделеева
3. Видеоурок:
· https://interneturok.ru/lesson/chemistry/11-klass/btipy-himicheskih-svyazejb/kovalentnaya-i-ionnaya-himicheskaya-svyaz?chapter_id=187&seconds=0
· https://www.youtube.com/watch?v=2yXsMaplB0E&feature=emb_title
4. Презентация:
· https://infourok.ru/prezentaciya-po-himii-na-temu-ionnaya-himicheskaya-svyaz-klass-2120061.html
· https://nsportal.ru/shkola/khimiya/library/2017/01/08/prezentatsiya-k-uroku-himii-v-8-klasse-ionnaya-svyaz
Ход урока
Каждый атом состоит из положительно заряженного ядра и отрицательно заряженной электронной оболочки. Благодаря зарядам ядра и электронов между соседними атомами возникают электростатические силы: притяжения и отталкивания. Если сближение атомов приводит к понижению энергии образующейся частицы (по сравнению с энергиями отдельных атомов), то образуется химическая связь.
Химическая связь – это силы взаимодействия, удерживающие частицы друг около друга.
Ученые доказали, что главную роль в образовании связи играют электроны, которые меньше всего связаны с ядром, т. е. расположенные на внешней электронной оболочке. Такие электроны называют валентными.
В атомах элементов главных подгрупп все валентные электроны расположены на последнем (внешнем) электронном слое и их число равно номеру группы.
В атомах элементов побочных подгрупп валентные электроны расположены, как правило, на двух последних электронных слоях, но их число тоже равно номеру группы, к которой относится элемент.
Например, в атоме калия один валентный электрон, в атоме марганца – 7 валентных электронов (рис. 1).

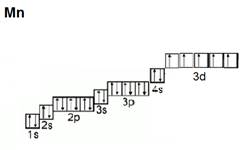
Рис. 1. Электронные конфигурации атомов калия и марганца
Согласно теории химической связи наиболее устойчивыми являются внешние оболочки из восьми электронов – октет (если в атоме только 1 электронный слой, то для него наиболее устойчиво двухэлектронное состояние – дуплет).
Образование устойчивой электронной оболочки может происходить несколькими способами, поэтому различают разные виды химической связи.
Представим, что встретились два атома: атом щелочного металла и атом галогена. У атома металла на внешнем энергетическом уровне — единственный электрон, а атому неметалла как раз не хватает одного электрона, чтобы завершить свой внешний уровень.
Атом металла легко отдаст свой слабо связанный с ядром валентный электрон атому неметалла, который предоставит ему свободное место на внешнем энергетическом уровне. Оба в результате получат заполненные внешние уровни.
Атом металла при этом приобретёт положительный заряд, а атом галогена превратится в отрицательно заряженнуючастицу. Такие частицы называются ионами.
Ионы — заряженные частицы, в которые превращаются атомы в результате отдачи или принятия электронов.
Образовавшиеся разноимённо заряженные ионы притягиваются друг к другу, и возникает химическая связь, которая называется ионной.
 2020-06-12
2020-06-12 461
461







