• Окислительно-восстановительные реакции органических веществ занимают важнейшее значение для процессов жизнедеятельности. С их помощью организм удовлетворяет свои энергетические потребности, поскольку при окислении органических веществ происходит высвобождение энергии.
• С другой стороны эти реакции служат для превращения пищи в компоненты клетки.
• Реакции окисления способствуют детоксикации и выведению лекарственных средств из организма.
• Окисление органических субстратов протекает тем легче, чем сильнее его тенденция к отдаче электронов.
• Окисление и восстановление необходимо рассматривать по отношению к определенным классам соединений.
• Выделяют три основные пути окисления:
• Горение 2СН4+3О2=2СО2+2Н2О
• Удаление водорода 2СН4=С2Н2+3Н2
• Образование более полярных связей СН4+[О]=СН3ОН
Окисление С – Н связей (алканов и алкилов)
Другие пути их окисления и восстановления можно представить следующими схемами:
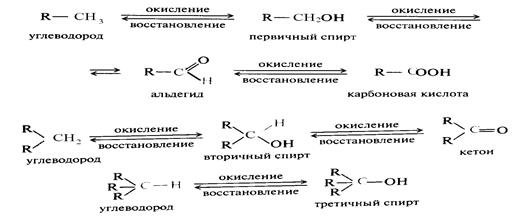
Окисление насыщенных углеводородов протекает в жестких условиях (горячая хромовая смесь) более мягкие окислители не действуют на них. Промежуточными продуктами окисления являются спирты, альдегиды, кетоны и кислоты.
• Гидропероксиды R – О – ОН важнейшие промежуточные продукты окисления С – Н связей в мягких условиях, в частности invivo
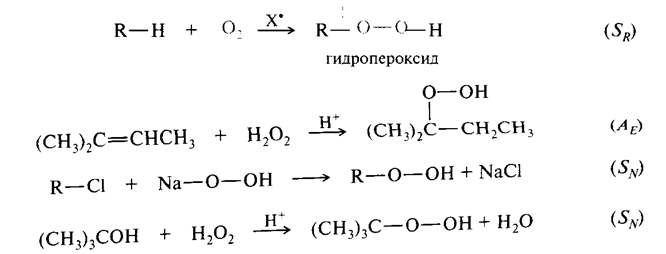 Важной реакцией окисления С – Н связей в условиях организма является ферментативное гидроксилирование.
Важной реакцией окисления С – Н связей в условиях организма является ферментативное гидроксилирование.
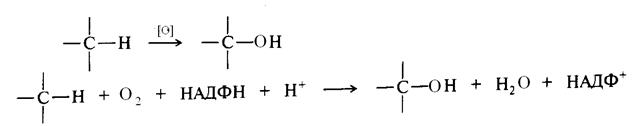
Примером может быть получение спиртов при окислении пищи. За счет молекулярного кислорода и его активных форм осуществляется в in vivo.
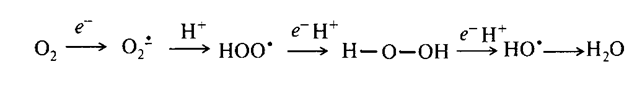 Перекись водорода может служить в организме гидроксилирующим агентом. Избыток перекиси должен разлагаться с помощью каталазы на воду и кислород.
Перекись водорода может служить в организме гидроксилирующим агентом. Избыток перекиси должен разлагаться с помощью каталазы на воду и кислород.
Н2О2=Н2О+О2
Окисление и восстановление алкенов можно представить следующими превращениями: 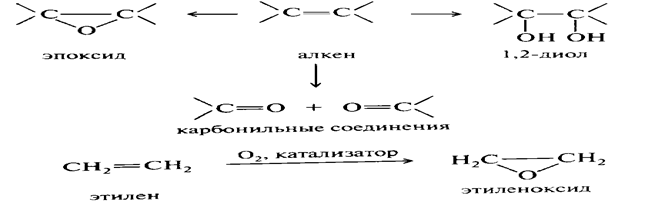
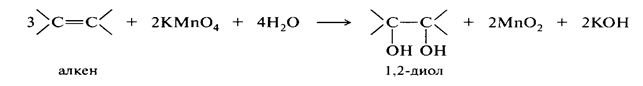
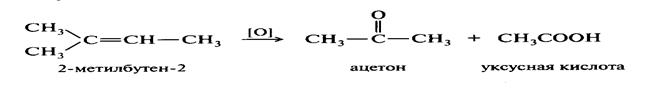
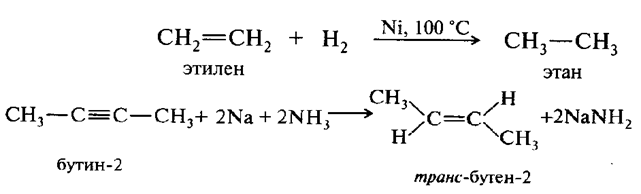
Восстановление алкенов
 2020-10-12
2020-10-12 265
265