А) Для письменного тестирования
Контрольные вопросы
Задание на СРСП
Сроки выполнения – 5-6 неделя. Виды заданий – реферат, контрольная работа.
Задание на СРС
1.Общие понятия о диаграммах состояния.
2. Диаграмма состояния воды.
3. Общие сведения о диаграммах состояния гетерогенных систем.
О [2] гл. VII, стр. 160- 164
Д [2] гл. VIII, 238-246
Д [4] стр. 189-201
1. Применение диаграмм состояния для решения технических задач.
О [2] гл. VI, стр. 165, 166, 168-170
Д [2] стр. 246-254
1. Какая система называется системой первого класса?
2. Что называется фазой?
3. Дайте определение правилу фаз Гиббса.
4. Как определяется число компонентов?
5. Для чего применяются уравнения Клаузиуса – Клапейрона?
Б) Тестовые задания по теме «Фазовые равновесия»
1. Фазой называется:
а) гомогенная часть системы;
б) гетерогенная часть системы;
в) поверхность;
г) термодинамическая система.
2. Систему, составные части которой не вступают в химические реакции, называют:
а) системой первого класса;
б) системой второго класса;
в) системой третьего класса;
г) системой открытой.
3. Двухкомпонентная система содержит:
а) два вещества;
б) одно вещество;
в) три вещества;
г) много веществ.
4. Вариантность определяется:
а) числом параметров состояния системы;
б) числом компонентов;
в) числом фаз;
г) изменением равновесия.
5. Укажите уравнение Клаузиуса – Клапейрона:
а) 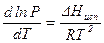 ;
;
б) F + n = K + 2;
в) Cv = (dU / dT)v;
г) Cp = (dH / dT)p.
6. Между составными частями системы идет взаимодействие, такая система называется:
а) системой второго класса;
б) системой первого класса;
в) системой третьего класса;
г) системой изолированной.
7. Однокомпонентная система содержит:
а) одно вещество;
б) два вещества;
в) много веществ;
г) четыре вещества.
8. Степени свободы – это:
а) независимые термодинамические параметры;
б) зависимые термодинамические параметры;
в) постоянные параметры;
г) переменные параметры.
9. Вариантность системы определяют:
а) по правилу фаз;
б) по правилу рычага;
в) по правилу Гиббса;
г) по формуле равновесия.
10. Скачкообразное изменение внутренней энергии, концентрации, плотности вещества приводит:
а) к фазовым превращениям первого рода;
б) к фазовым превращениям второго рода;
в) фазовые превращения не происходят;
г) к изменению теплоты.
| № | Русс/каз/англ. | Пояснение |
| Фазовое равновесие | Переход компонентов из одной фазы в другую | |
| Фазалық тепе-тендік | ||
| Phase equilibrium | ||
| Фаза | Гомогенная часть системы | |
| Фаза | ||
| Phase | ||
| Система | Тело или группа тел, выделяемых для рассмотрения | |
| Жүйелер | ||
| System | ||
| Число компонентов | Показывает число независимых составных частей системы | |
| Компоненттер саны | ||
| Component number | ||
| Степень свободы | Независимые термодинамические параметры фаз системы | |
| Еркіндік дәрежесі | ||
| Iveedom degree | ||
| Правило фаз | Принцип классификации равновесий в сложных гетерогенных системах | |
| Фазалар ережесі | ||
| Vike phase (stage) | ||
| Двухфазные системы | Двухфазные системы состоят из двух фаз | |
| Екі фазалы жүйелер | ||
| Diphasic systems |
 2014-02-02
2014-02-02 894
894








