Важно:изложенные далее закономерности относятся ко всем реакциям нуклеофильного замещения в производных алканов, а не только к гидролизу галогеноалканов. Т.е. ко всем взаимодействия с нуклеофлами (например с: NH3, -NH2, Cl-, HS- и др.) и ко всем уходящим группам.
Гидролиз галогена в бромметане приводит к метанолу:
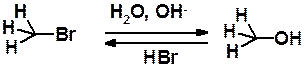
Кинетические исследования показали, что скорость этой реакции зависит от концентрации обоих реагентов:
V = k[CH3Br][OH-]
Такое взаимодействие называют реакцией второго порядка или бимолеклярной (сумма стехиометрических коэффициентов 1 + 1 = 2).
Внешне очень похож на приведенную выше реакцию гидролиз брома в трет -бутилбромиде:
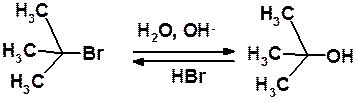
Скорость этой реакции зависит от концентрации бромопроизводного и не зависит от концентрации нуклеофила:
V = k[(CH3)3Br]
Вывод: реакции протекают по различным механизмам!
Бимолекулярное нуклеофильное замещение (SN2)
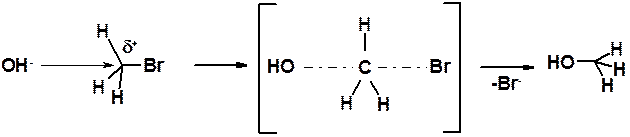
Реакция идет в одну стадию, через единственное переходное состояние (в квадратных скобках), в котором связь С-О еще полностью не образовалась, а связь С-Br еще полностью не разорвалась (показаны пунктиром). Нуклеофил всегда атакует с противоположной стороны от уходящей группы («атака с тыла»).

Рис. 22.2. Энергетическая диаграмма реакции SN2
Мономолекулярное нуклеофильное замещение (SN1)
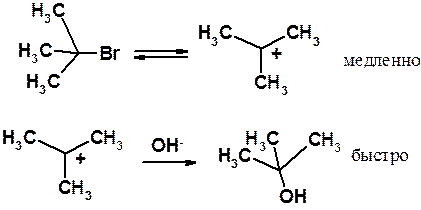
Трет -бутилбромид медленно диссоциирует на карбокатион и Br-. Образовавшийся карбокатион очень быстро (практически мгновенно) реагирует с гидроксид-анионом.
Хотя скорость реакции равна сумме скоростей первой и второй стадий, первая протекает во много раз медленнее, чем вторая, вкладом которой в суммарную скорость реакции можно пренебречь. Стадия, скорость которой определяет скорость всей реакции, называется лимитирующей. В рассмотренной реакции именно первая стадия, проходящая с поглощением энергии (см. рис. 22.3), является лимитирующей. В этой стадии принимает участие только молекула галогенопроизводного. Именно его концентрация определяет скорость всей реакции.
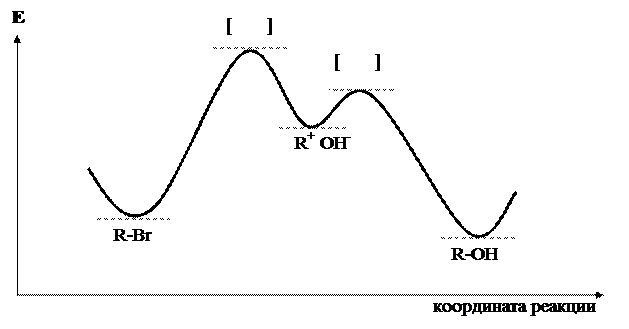 |
Рис. 22.3. Энергетическая диаграмма реакции SN1
Мономолекулярные реакции часто осложняются побочными процессами, связанными со склонностью карбокатионов к перегрппировкам.
Так, гидролиз 1-хлор-2-метилпропана в результате 1,2-гидридного сдвига приводит не к 2-метилпропанолу-1, а к трет -бутанолу.
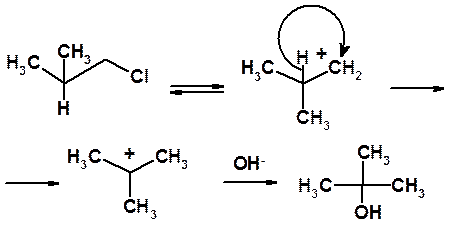
В реакции 1-бром-2,3-диметилпропана с этанолом в результате 1,2-метильного сдвига образуется не к 2,3-диметилпропанолу-1, а 2-метил-2-этоксибутан и метилбутен-2.
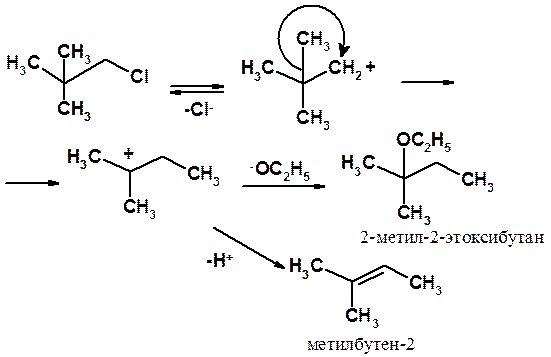
Строгое доказательство протекания реакций SN1 и SN2 по указанным выше механизмам дает совокупность данных кинетических измерений и исследования стереохимических особенностей протекания реакций.
 2014-02-02
2014-02-02 1355
1355







