Термодинамические потенциалы
Изменение энтропии однозначно определяет направление и предел самопроизвольного протекания процесса только для изолированных систем: если в результате расчета окажется, что D S > 0, процесс пойдет самопроизвольно, при D S = 0 – состояние равновесия, если D S < 0, процесс самопроизвольно протекать не будет.
На практике приходится иметь дело преимущественно с системами, взаимодействующими с окружающей средой. В качестве критерия оценки направления самопроизвольных процессов в таких системах используются термодинамические потенциалы.
Термодинамическим потенциалом называют функцию состояния, убыль которой в обратимо протекающем процессе при постоянстве определенных параметров равна максимальной полезной работе.
Наибольшее значение имеют два основных термодинамических потенциала: энергия Гельмгольца F (T, V) и энергия Гиббса G (T, p). В скобках указаны параметры, функциями которых являются термодинамические потенциалы.
Чтобы получить представление о термодинамических потенциалах, воспользуемся объединенным математическим выражением первого и второго законов термодинамики.
I закон термодинамики:
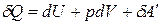 .
.
II закон термодинамики:
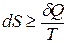 или
или 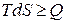 .
.
Объединенное математическое выражение:
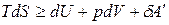 ,
,
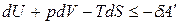 . (6)
. (6)
Рассмотрим соответствующие процессы.
1. Изобарно-изотермический процесс (p, T = const).
Уравнение (6) запишется (из математики: любую константу можно внести под знак дифференциала, а сумма дифференциалов равна дифференциалу от суммы)
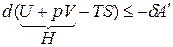 ,
,
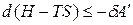 ,
,
где H – TS = G –свободная энергия Гиббса. При p, T = const изменение энергии Гиббса связано с выполнением полезной работы:
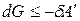 .
.
В обратимо протекающем процессе 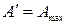 . Тогда
. Тогда
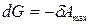 ,
,
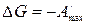 .
.
Таким образом, свободная энергия Гиббса является изобарно-изотермическим потенциалом, так как ее уменьшение характеризует максимальную работу этого процесса.
Если единственным видом работы является работа расширения (сжатия), т.е. 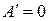 , то в необратимом, а, следовательно, самопроизвольно протекающем процессе
, то в необратимом, а, следовательно, самопроизвольно протекающем процессе
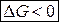 . (7)
. (7)
2. Изохорно-изотермический процесс (V, T = const, pdV = 0).
Уравнение (6) примет вид
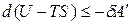 ,
,
где U – TS = F – свободная энергия Гельмгольца. При V, T = const изменение энергии Гельмгольца связано с выполнением полезной работы:
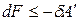 .
.
В обратимо протекающем процессе
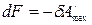 ,
,
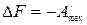 .
.
Таким образом, свободная энергия Гельмгольца является изохорно-изотермическим потенциалом.
Если 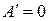 , то в самопроизвольно протекающем процессе
, то в самопроизвольно протекающем процессе
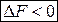 . (8)
. (8)
Неравенства (7), (8) являются условием самопроизвольного протекания процесса при постоянстве соответствующих параметров: самопроизвольно могут протекать только те процессы, которые приводят к понижению свободной энергии системы; система приходит в состояние равновесия, когда свободная энергия достигает минимального значения.
 2014-02-12
2014-02-12 996
996








