Пропанон-2
Г. Восстановление альдегидов, кетонов, эфиров
Этилхлорид Этанол
В. Гидролиз галогенпроизводных
Методы получения и химические свойства
Одноатомные предельные спирты.
Физические свойства спиртов
Изомерия
Номенклатура спиртов
Для спиртов существует несколько способов их названия. При названии отдельных спиртов широко применяются исторические названия (тривиальные): древесный спирт СН3ОН, С2Н5ОН – винный спирт.
По радикально-функциональной номенклатуре алифатические спирты с прямой углеродной цепью называют по наименованию радикала, например С2Н5ОН этиловый спирт.
СН3 –СН2 – ОН – этиловый спирт,
СН3 – СН2 –СН2 – ОН – пропиловый спирт
По систематической номенклатуре ИЮПАК:
– выбирают самую длинную цепь, содержащую функциональную ОН-группу;
– названия спиртов образуются от названий соответствующих углеводородов с добавлением суффикса – ол (для одноатомных), -диол (для 2-х атомных), -триол (3-х атомных), в необходимых случаях положение гидроксильной группы обозначается номером.
2 1
СН3 – СН2 – СН2 – СН2 – ОН – 4-хлор-2-этилбутанол-1
|3 4
СН2 –СН2–Сl
СН2 –СН2 – СН2 – СН2 – СН3 пентандиол-1,2 (гликоль)
| |
ОН ОН
1 2 3
СН2 – СН –СН2 – прапантриол-1,2,3, (Глицерин)
| | |
ОН ОН ОН
Изомерия спиртов обусловлена строением углеводородного радикала и положением функциональной (гидроксильной) группы. Например, молекулярной формуле С4Н10ОН соответствуют четыре спирта:
| СН3 – СН 2 – СН 2 – СН 2 –ОН 1-бутанол, (н-бутанол) | СН3 – СН – СН2 – СН3 | 2-бутанол, ОН (втор-бутиловый спирт) |
| СН3 | СН3 – СН –СН2 –ОН 2-метил-1-пропанол, (изо-бутиловый спирт) | СН3 | СН3 – СН –СН3 | 2-метил-2-пропанол, ОН (трет-бутиловый спирт) |
Низшие и средние члены гомологического ряда предельных одноатомных с С1 до С11 спиртов – жидкости, высшие (начиная с С11) – твердые вещества. Плотности предельных и непредельных одноатомных спиртов меньше единицы. У ароматических спиртов немного больше единицы. Первые три члена (метанол, этанол, пропанол) имеют характерный запах и жгучий вкус, смешиваются с водой в любых соотношениях. Высшие спирты, так же как и высшие углеводороды, практически нерастворимы в воде.
3.1 Методы получения
А. Гидратация алкенов:
СН3–CH=CH2+HOН---------------------® СН3–CH–CH3
[H3PO4], T=3000C, P |
OH
Б. Ферментативное брожение углеводов:
Углеводы (глюкоза, сахароза, крахмал) ----------------®
Био-катализаторы (ферменты)
® С2Н5ОН (этанол) + (побочные продукты: пропиловый, бутиловый, амиловый спирты)
CH3– CH2–Cl + HOH® CH3– CH2–OH + HCl
– из альдегидов
CH3– CОН + Н2 -------® CH3– CH2–OH
Уксусный альдегид (Pt, Ni) Этанол
– из кетонов (получаются вторичные спирты)
СН3 – С –СН3 + Н2 -------® СН3 – СН –СН3
|| (Pt)|пропанол-2
О ОН
3.2 Химические свойства предельных спиртов
Свойства спиртов определяется строением гидроксильной группы, характером ее химических связей, строение углеводородных радикалов и их взаимным влиянием. Связи О–Н и С–О – полярные ковалентные. Электроотрицательность атома кислорода (3,5), водорода (2,1), углерода (2,4). Электронная плотность обеих связей смещена к наиболее электроотрицательному атому кислорода. Атому кислорода в спиртах свойственна Sp3–гибридизация. В образовании его связей С и Н участвуют Sp3–атомные орбитали, валентный угол С–О–Н близок к тетраэдрическому (около 108,50). Каждая из двух Sp3–АО кислорода занята неподеленной парой электронов.
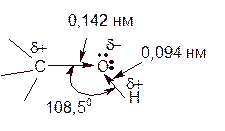
Предельные одноатомные спирты – практически нейтральные вещества. Они не изменяют окраски индикаторов, не вступают в реакцию ни сводным раствором щелочей, ни с разбавленными кислотами.
Однако в определенных реакциях спирты все же проявляют свойства очень слабых кислот и оснований, т.е. являются амфотерными подобно воде.
Таблица 2 – Кислотные и основные свойства спиртов
| Соединение | Кдис |
| Н–ОН | 1,8*10-16 |
| Н2СО3 (угольная кислота) | 4,9*10-7 |
| СН3СООН (уксусная кислота) | 1,8*10-5 |
| С2Н5ОН (спирт) | 1,0*10-18 |
| С6Н5–ОН (фенол) | 1,3*10-10 |
 2014-02-13
2014-02-13 1783
1783








