Хотя скорость некоторых химических реакций описывается кинетическим уравнением третьего порядка, это еще не значит, что они действительно тримолекулярные. Однако оно удобно для вывода кинетического уравнения: 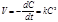 . (8.24) После интегрирования получим:
. (8.24) После интегрирования получим: 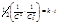 или
или 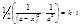 , (8.25)
, (8.25)
если а – исходная концентрация, (а - х) – количество вещества, оставшегося ко времени t. Если реакция протекает по уравнению: 2А + В ® продукты и если [ B ] не равна [ A ], то интегрирование выражения для скорости реакции третьего порядка значительно усложняется.
Уравнение скорости реакции нулевого порядка. Если в уравнении скорости отсутствуют члены, содержащие концентрацию реагирующих веществ, то скорость такой реакции выражается уравнением нулевого порядка 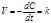 . (8.26) Реакция нулевого порядка представляет особый интерес в каталитических процессах, когда катализатор, взятый в определенном количестве, может служить фактором, лимитирующим скорость реакции. Такая ситуация встречается в ферментативной кинетике.
. (8.26) Реакция нулевого порядка представляет особый интерес в каталитических процессах, когда катализатор, взятый в определенном количестве, может служить фактором, лимитирующим скорость реакции. Такая ситуация встречается в ферментативной кинетике.
 2015-02-04
2015-02-04 741
741








