Задача 1. Бимолекулярная реакция, для которой исходные концентрации реагентов равны, протекает за 10 мин на 25%. Сколько потребуется времени, чтобы реакция прошла на 50% при той же температуре?
Решение:
Запишем выражения константы скорости реакции для t1 и t2.
К= 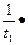
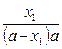 ; К=
; К= 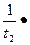
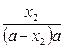
Правые части уравнений равны:
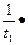
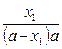 =
= 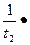
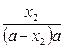
После сокращения и подстановки числовых значений
Х1 = 0,25•а и Х2 = 0,5•а получаем:
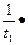
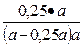 =
= 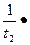
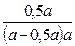 или
или 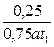 =
= 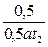
Откуда t2 = 30 мин.
Ответ: 30 мин.
Задача 2. Константа скорости реакции второго порядка
СН3СООС2Н5 + NaOH →- CH3COONa + С2Н5ОН
а b
равна 5,4 л/моль с. Сколько эфира прореагирует за 10 мин. при а=b= 0,02моль/л?
Решение:
КП=  ∙
∙ 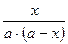 , отсюда находим х
, отсюда находим х
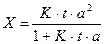 t = 10 мин. = 600 с
t = 10 мин. = 600 с 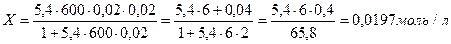
Ответ: 0,0197 моль/л
Задача 3. Изучалась реакция. В результате получены следующие данные:
t мин 5 10
х моль/л 0,010 0,020
Исходная концентрация была равна 0,219 моль/л. Определите порядок реакции.
Решение:
Предположим, что это реакция первого порядка, тогда рассчитаем К по формуле: 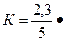 lg
lg 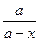
K1= 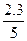 lg
lg 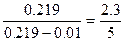 lg
lg 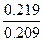

К, = 0,46 lg 0,219 - 0,46 lg 0,209
К, = 0,46 (1,3404) - 0,46 (1,3201)
К, = 0,46 (-0,6596) - 0,46 (-0,6799)
К, = 0,46•0,6799 - 0,46•0,6596 = 0,46 (0,6799 - 0,6596)
Ki = 0,46•0,0203 = 0,009338
К, = 9,338•10 -3 К2= 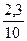 lg
lg 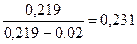 lg
lg 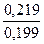
К2 = 0,23 lg0,219-0,23 lg0,199
К2 = 0,23• lg0,3404 - 0,23• lg0,2989
К2 = 0,23(lg0,3404 - 0,23• lg0,2989) = 0,23•0,0415 = 9,5•10 -3
Ответ: Константы приблизительно равны, следовательно, изучаемая реакция первого порядка.
Задача 4. Реакция первого порядка протекает на 30 % при температуре 25°С за 30 минут, а при температуре 40°С за 5 минут. Найдите энергию активации (Е).
Решение:
Т1 = 273 + 25 = 298°К Т2 = 273+40 = 313°К
К289= 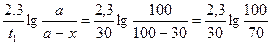
К313= 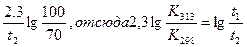
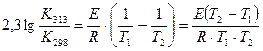 ,отсюда
,отсюда
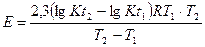
R = 8,315 Дж/моль 0К
К298= 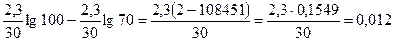
lgK298= 2,0792
К313= 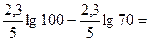 0,46(2-1,8451) = 0,46•0,1549 = 0,071245 lgK313 = 2,8528
0,46(2-1,8451) = 0,46•0,1549 = 0,071245 lgK313 = 2,8528
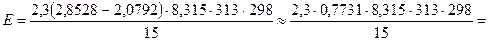 9,1934 Дж/ моль
9,1934 Дж/ моль
Ответ: 9,1934 Дж/ моль
 2015-02-04
2015-02-04 13901
13901








