Результаты испытания записывают в табл. 19, 20 и обрабатывают их математически, и графически.
Таблица 19
Марка стали ___________________
Термообработка ___________________
Линейные размеры образцов ___________________________ мм
Точность взвешивания _________________________ г
Температура раствора _____________
Продолжительность испытаний ________________ ч
| Электролит | Номер образца | S, м2 | Масса образца, г | Km, г/м2·ч | Z±ΔZ, % | γ | Результаты наблюдений за раствором и образцом | |
| до коррозии m 0 | после коррозии m 1 | |||||||
Таблица 20
Материал образца _______________
Электролит _____________________
Поверхность катода S к __________________ см2;
Поверхность анода S а __________________ см2.
| Начальный ток I, мА | Потенциал катода | Ток после измерения потенциала катода I 1, мА | i к, мА/м2 | Потенциал анода | Ток после измерения потенциала катода I 2, мА | i a, мА/м2 | ||
| по х.с.э., Е хсэк, В | по н.в.э., Е к, В | по х.с.э., Е хсэа, В | по н.в.э., Е а, В | |||||
Показатель изменения массы (весовой показатель коррозии, г/м2·ч) рассчитывают по уравнению:
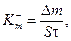 (95)
(95)
где Δ m – уменьшение массы металла в результате коррозии, г; S – поверхность образца, м2; τ – время коррозии металла, ч.
Проводят статистическую обработку результатов исследования (пример приведен в конце работы).
Эффективность действия Z рассчитывают по формуле (93), защитный эффект γ – по формуле (94).
Потенциал металла по отношению к стандартному водородному электроду рассчитывают по формуле:
Е Ме = Е хсэМе + Е хсэ, (96)
где Е Ме – потенциал металла по отношению к стандартному водородному электроду, В; Е хсэ – потенциал хлорсеребряного электрода сравнения при температуре опыта, В; Е хсэМе – потенциал металла по отношению к хлорсеребряному электроду, В.
По полученным данным строят графики зависимости Е Ме = f(i а) и Е к = f(i к) для раствора без ингибитора и с ингибитором. На основании поляризационных кривых стали в кислоте с ингибитором и без него определяют механизм действия ингибитора.
 2015-03-22
2015-03-22 318
318








