В огромном ряду материалов, с незапамятных времен известных человеку и широко используемых им в своей жизни и деятельности, металлы всегда занимали особое место. Подтверждение этому: и в названиях эпох (золотой, серебряный, бронзовый, железный века), на которые греки делили историю человечества: и в археологических находках металлических изделий (кованые медные украшения, сельскохозяйственные орудия); и в повсеместном использовании металлов и сплавов в современной технике. Причина этого - в особых свойствах металлов, выгодно отличающих их от других материалов и делающих во многих случаях незаменимыми.
Металлы – один из классов конструкционных материалов, характеризующийся определенным набором свойств:
- «металлический блеск» (хорошая отражательная способность);
- пластичность;
- высокая теплопроводность;
- высокая электропроводность.
Данные свойства обусловлены особенностями строения металлов. Электроны в металлах имеют возможность перемещаться по всему объему металла, т.е. принадлежат целой совокупности атомов. Таким образом, пластичность, теплопроводность и электропроводность обеспечиваются наличием «электронного газа».
Все металлы, затвердевающие в нормальных условиях, представляют собой кристаллические вещества, то есть укладка атомов в них характеризуется определенным порядком – периодичностью, как по различным направлениям, так и по различным плоскостям. Этот порядок определяется понятием кристаллическая решетка.
Кристаллическая решетка (рис. 1) - это воображаемая пространственная решетка, в узлах которой располагаются частицы, образующие твердое тело. Элементарная ячейка кристаллической решетки – элемент объема из минимального числа атомов, многократным переносом которого в пространстве можно построить весь кристалл. Элементарная ячейка характеризует особенности строения кристалла. Основными параметрами кристалла являются:
- периоды решетки (a, b, c) – расстояния между центрами ближайших атомов;
- координационное число (К) указывает на число атомов, расположенных на ближайшем одинаковом расстоянии от любого атома в решетке;
- плотность упаковки атомов в кристаллической решетке. Ее определяют как отношение объема, занятого атомами, к объему ячейки.
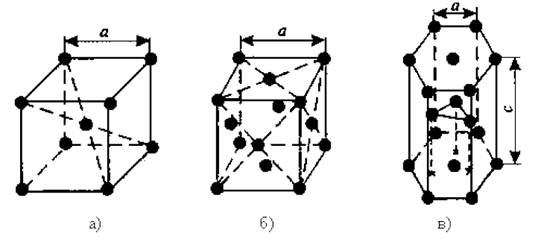
Рис. 1. Основные типы кристаллических решеток металлов: а – объемно-центрированная кубическая; б – гранецентрированная кубическая; в – гексагональная плотноупакованная
Основными типами кристаллических решеток металлов являются:
1. Объемно-центрированная кубическая (ОЦК) (рис.1а), атомы располагаются в вершинах куба и в его центре (V, W, Ti);
2. Гранецентрированная кубическая (ГЦК) (рис. 1б), атомы располагаются в вершинах куба и по центру каждой из 6 граней (Ag, Au);
3. Гексагональная плотноупакованная (ГПУ) (рис. 1в).
В кристаллических телах атомы правильно располагаются в пространстве, причем по разным направлениям расстояния между атомами неодинаковы, что предопределяет существенные различия в силах взаимодействия между ними и, в конечном результате, разные свойства. Зависимость свойств от направления называется анизотропией.
Анизотропия проявляется только в пределах одного кристаллического зерна. Реальные металлы являются телами поликристаллическими, состоящими из огромного числа зерен, произвольно ориентированных друг к другу своими кристаллографическими направлениями и плоскостями. Поэтому они являются изотропными телами, т.е. телами с примерно одинаковыми свойствами по всем направлениям.
Способность некоторых металлов существовать в различных кристаллических формах в зависимости от внешних условий (давление, температура) называется аллотропией или полиморфизмом. Используя явление полиморфизма, можно упрочнять и разупрочнять сплавы при помощи термической обработки.
В кристаллической решетке реальных металлов имеются различные дефекты (несовершенства), которые нарушают связи между атомами и оказывают влияние на свойства металлов.
Одним из распространенных несовершенств кристаллического строения является наличие точечных дефектов: вакансий, дислоцированных атомов и примесей (рис. 2).
Вакансия – отсутствие атомов в узлах кристаллической решетки, «дырки», которые образовались в результате различных причин.
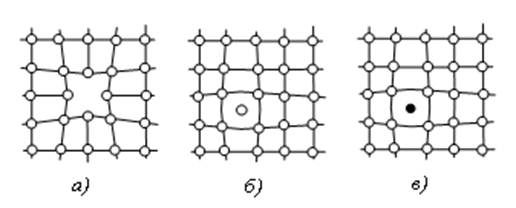
Рис. 2. Точечные дефекты кристаллов: а – вакансия, б – дислоцированный атом, в – примесный атом
Дислоцированный атом – это атом, вышедший из узла решетки и занявший место в междоузлие. Концентрация дислоцированных атомов значительно меньше, чем вакансий, так как для их образования требуются существенные затраты энергии. При этом на месте переместившегося атома образуется вакансия.
Примесные атомы всегда присутствуют в металле, так как практически невозможно выплавить химически чистый металл. Они могут иметь размеры больше или меньше размеров основных атомов и располагаются в узлах решетки или междоузлиях.
Вопросы для самоконтроля
4.1.Перечислите характерные свойства металлов.
4.2.Что такое кристаллическая решетка?
4.3. Основные параметры кристаллической решетки?
4.4. Что такое анизотропия?
4.5. Что такое полиморфизм?
4.6. Какие виды кристаллических решеток характерны для металлов?
4.7. Охарактеризуйте основные виды точечных дефектов кристаллической решетки.
 2015-03-07
2015-03-07 880
880








