В5. Установите соответствие между схемой химической реакции, протекающей в растворе, и суммой коэффициентов в молекулярном уравнении реакции.
Ответ запишите в виде сочетания букв и цифр, соблюдая алфавитную последовательность букв левого столбца, например: А4Б1В2Г6.
| Схема реакции | Сумма коэффициентов в молекулярном уровнении | |
| А) Fe + HCl | 1) 3 | |
| Б) Ca(OH)2 + HBr(изб.) | 2) 4 | |
| В) AgF + KI | 3) 5 | |
| Г) Zn(OH)2 + KOH | 4) 6 | 5) 7 |
Решение:
А. Fe + 2 HCl ® Fe Cl2 + H 2
A3 S 5
Б. Ca (OH)2 + 2 HBr ® Ca Br2+ 2 H2O
Б4. S6
В. Ag F + K I ® Ag I¯ + KF
B2 S4
Г. Zn (OH)2 + 2 KOH ® K 2[Zn(OH)4]
Г2 S 4
Ответ: А3Б4В2Г2
В6. Известны тепловые эффекты следующих процессов:
2С2Н2(г) + 5О2(г) ® 4СО2(г) + 2Н2О(ж) + 2600 кДж
Н2О(ж) ® Н2О(г) – 40 кДж
Какую массу воды можно испарить за счет теплоты, полученной при полном сгорании 89600 см3 (н.у.) этина С2Н2?
Решение:
Х кДж
2С2Н2(г) + 5О2(г) = 4СО2(г) + 2Н2О(ж) + 2600 кДж
2∙22,4
х =89,6×2600/(2 × 22,4)=5200 кДж;
Х 5200 кДж
Н2О(ж) = Н2О(г) – 40 кДж.
х = 18×5200:40 = 2340 (г)
Ответ: 2340
В7. Смесь малахита (Сu(OH)2 × CuCO3), гидроксида меди (II) и карбоната меди(II) общей массой 297г прокалили до прекращения изменения массы и получили 200г твердого остатка. Определите объем (дм3, н.у.) выделившегося при этом углекислого газа.
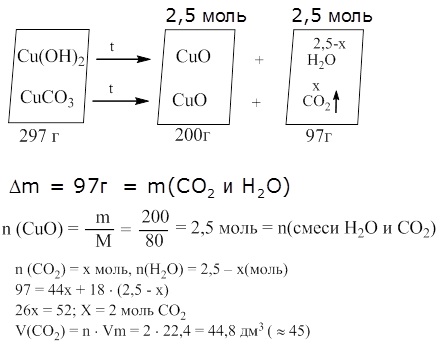
 2015-03-08
2015-03-08 1444
1444








