Обычно говорят об s-, p-, d-, f-подуровнях, s-, p-, d-, f-электронных облаках (рис. 2.1) и, соответственно, об s-, p-, d-, f-электронах.
 |  | ||
 |  | ||
 |  |
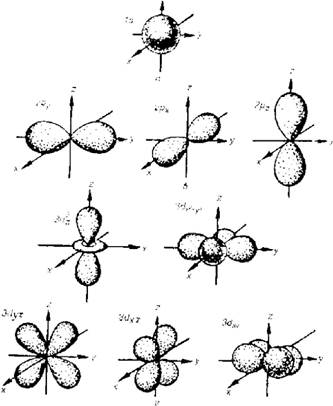 |
s-облако
р-облака
d-облака
Рис. 2.1. Форма электронных облаков различных атомных орбиталей
Граничная поверхность s-электрона представляет собой сферу, у р-облаков форма гантелей, или объемных восьмерок, расположенных вдоль каждой из координатных осей, у d-электронов четыре облака имеют форму четырехлопастных лепестков, а пятое - форму объемной восьмерки с пояском по центру (рис. 2.1).
Электронное облако не имеет четко очерченных границ в пространстве. Можно говорить лишь о его плотности, о вероятности пребывания электрона в каждой фиксированной точке пространства, которая определяется квадратом
абсолютного значения волновой функции l^) 2. Обычно проводят граничную
поверхность, которая заключает около 90 % заряда и массы электрона.
При записи цифрой указывается главное квантовое число, а затем буквой - орбитальное квантовое число. Например, 2р означает, что у электрона п = 2, / = 1; 3d означает, что п = 3, / = 2.
По энергетическим подуровням происходит возрастание энергии электронов в следующем порядке:
I s < 2s < 2 р < 3s < Зр < 4s < 3d < 4 р < 5s < 4d < 5 р < 6s < 4f * * 5d < 6p < 7s < 5f * 6d < 7p,
 2015-04-01
2015-04-01 821
821








