Чтобы понять, как устроена жизнь, в первую очередь необходимо было установить, из каких компонентов состоит живая материя и что её в этом отношении отличает от материи неживой. Затем требовалось определить, какие из этих компонентов отвечают за самое важное свойство живого — передачу наследственных свойств от родителей потомкам.
Конечно, в наше время бурного развития биологии ответы на эти вопросы кажутся яснее ясного, однако всего несколько десятилетий назад учёным пришлось немало поломать над ними головы.
Тот факт, что живая материя отличается от неживой по составу, был очевиден уже для естествоиспытателей древности. Всё живое более хрупко и неустойчиво — отмечали они. Если сильно нагреть что-либо неживое — воду или камень, они после остужения снова превращают ся в исходную форму. Если то же проделать с живым — оно либо меняется, либо разрушается. Какие же вещества определяют эту существенную разницу?
В течение примерно сотни лет химики накапливали знания о структуре жизни. Обобщил эти познания английский физиолог Уильям Прут. В 1827 году он впервые назвал три основные группы веществ, которые отличают живую материю: углеводы (карбогидраты), жиры (липиды) и белки (протеины).
Белки оказались наиболее сложно устроенными молекулами жизни. Кроме углерода, кислорода и водорода белки содержат значительные количества азота и серы, а некоторые из них способны прочно удерживать атомы определённых металлов, таких, как цинк или железо. Неудивительно, что именно белки привлекли особое внимание исследователей жизни, и не только потому, что они так сложно устроены. Вскоре произошли открытия, позволившие считать белки центральной, самой важной из всех „жизненных“ молекул.
Одна из характерных черт живого — подвижность — привлекала внимание человека задолго до открытия белков. В XVII–XVIII веках учёные выяснили, что причина этого в химических реакциях, которые в организме идут значительно быстрее, чем в неживой природе. Углекислый газ и вода в клетках растений быстро превращаются в сахара, белки и жиры, а те, будучи съедены животными, позволяют им быстро двигаться и строить новые белки, сахара и жиры для собственных клеток.
Постепенно становилось понятным, что какой-то механизм ускоряет химические реакции в живой материи и делает её резко отличной от всего неживого. Вещества, способные ускорять химические реакции, — катализаторы (от греческого слова, означающего „разрушение“) были известны ещё с XVIII века. Они, хотя и остаются неизменными в конце реакции, обладают способностью её многократно ускорять. Химики предположили, что по аналогии с превращениями неорганических веществ такие же катализаторы могут присутствовать и в живых тканях, ускоряя процессы метаболизма. Гипотеза блестяще подтвердилась в 1833 году, когда французский химик Ансельм Пайен (1795–1871) выделил из проросшего зерна вещество, которое он назвал „диастаз“. Диастаз обладал свойствами превосходного катализатора: в его присутствии крахмал из зёрен разлагался на простые сахара во много раз быстрее.
Как вы уже, наверное, догадались, и диастаз, и великое множество биологических катализаторов, открытых после него, оказались белками. Им было дано специальное название — ферменты (или энзимы), что переводится с двух великих древних языков, латинского и греческого, одинаково — „закваска“.
С момента обнаружения этих замечательных свойств молекула белка поднялась на недосягаемую высоту и стала считаться „эссенцией жизни“. Неудивительно, что именно белок стал первым кандидатом на звание прародителя всех организмов. Без белка немыслима жизнь, а значит, как казалось учёным, немыслимо и само её зарождение.
 В 1924 году А.И. Опарин (1894–1980) высказал предположение, что в атмосфере молодой Земли, состоявшей из водорода, метана, аммиака, углекислого газа и паров воды, могли синтезироваться аминокислоты, которые затем спонтанно соединились в белки и образовали „сгустки“, напоминающие примитивную клетку. В 1924 году А.И. Опарин (1894–1980) высказал предположение, что в атмосфере молодой Земли, состоявшей из водорода, метана, аммиака, углекислого газа и паров воды, могли синтезироваться аминокислоты, которые затем спонтанно соединились в белки и образовали „сгустки“, напоминающие примитивную клетку. |
Окончательно такие представления о „белково-клеточных“ истоках жизни оформились в теории, созданной в 20-х годах XX века советским биохимиком А.И. Опариным и английским исследователем Дж. Холдейном. Они предположили, что в условиях молодой Земли, где, по современным представлениям, атмосфера состояла из метана, углекислого газа, циановодорода, молекулярного водорода и была насыщена парами воды, могли спонтанно образовываться аминокислоты — основные структурные молекулы, из которых состоят все белки. Представить такой процесс несложно: ведь аминокислоты достаточно просты по строению (забегая вперёд, скажем, что возможность образования аминокислот из неорганических компонентов была впоследствии подтверждена экспериментально). Затем, по мысли авторов гипотезы, такие аминокислоты могли объединяться, образуя короткие молекулы белков. Те, в свою очередь, „склеиваясь“ друг с другом, образовывали сгустки (коацерваты), свободно плавающие в первобытном океане. Такие коацерваты, возможно, могли расти, и от них могли отделяться дочерние коацерваты. При этом наверняка у некоторых из белковых молекул могли проявляться свойства ферментов. Таким образом, коацерватный сгусток явно напоминал примитивную клетку. Теория Опарина-Холдейна стала необычайно популярной.
Существовал, однако, один важнейший вопрос, на который сторонники белкового происхождения жизни долгое время закрывали глаза: как могли белки, обладающие полезными свойствами ферментов, хранить и передавать информацию об этих полезных свойствах другим белкам? Иными словами: как мог осуществляться механизм наследственности? И здесь снова необходимо небольшое отступление в историю науки.
Опубликованный в 1859 году эпохальный труд Чарльза Дарвина „Происхождение видов путём естественного отбора“ указал на особую важность процессов изменчивости и наследственности в эволюции живого. Тут же начались интенсивные поиски материальных носителей этих механизмов. Что определяет „признак“, например цвет глаз, кожи или волос у животных? Почему дети похожи на своих родителей? Почему, благодаря какому механизму сохраняются и передаются свойства клеток и целых организмов?
В 40-х годах XIX века Маттиас Шлейден, один из отцов положения об универсальности клеточного строения всего живого, не имея в своём распоряжении достаточно хороших линз для микроскопа, описывал образование дочерней клетки как „отпочковывание“ её от ядра клетки-родительницы. Хотя это наблюдение было вскоре признано неверным, авторитет Шлейдена заставил учёных внимательнее изучить процессы, происходящие в ядре клеток. В 70-х годах того же XIX века немецкий цитолог Уолтер Флемминг заметил, что при окрашивании клетки одним из синтетических красителей внутри ядра можно обнаружить пятна, окрашенные гораздо сильнее, чем окружающее вещество. Флемминг назвал окрашенную субстанцию хроматином (от греческого слова „цвет“ или „цветной“). В процессе клеточного деления строение хроматина менялось: он распадался на ряд хорошо видных отдельных телец, названных хромосомами. В самом начале XX века американский биолог Уолтер Саттон обнаружил, что поведение хромосом хорошо согласуется с распределением наследственных признаков, как их описал основоположник генетики Грегор Мендель: каждый вид характеризуется строго определённым числом хромосом, которое сохраняется у потомков; при половом размножении в дочернюю клетку всегда попадает одна хромосома от отца и одна от матери.
Постепенно становилось ясно, что именно в хромосомах следует искать „материал наследственности“. Что же он собой представляет?
В конце XIX века было показано, что и хроматин и хромосомы состоят из белков и молекул нуклеиновых кислот (от слова „нуклеус“ — ядро). Как мы уже знаем, незадолго до Дарвина были открыты удивительные свойства белков, поэтому не приходится удивляться, что из двух возможных претендентов на звание носителя наследственности учёный мир, нимало не сомневаясь, выбрал белки. На некоторое время именно белки в хромосомах стали считать ответственными за передачу наследственных признаков. Отчасти это объясняет и выбор белков как носителей информации в теории Опарина и Холдейна: ведь истинный „носитель“ в момент создания теории ещё не был найден.
 Американский биолог Освальд Эвери убедительно продемонстрировал в опытах с бактериями, что именно нуклеиновые кислоты отвечают за передачу наследственных свойств. Американский биолог Освальд Эвери убедительно продемонстрировал в опытах с бактериями, что именно нуклеиновые кислоты отвечают за передачу наследственных свойств. |
Положение кардинально изменилось лишь в 1944 году, когда учёные под руководством американского бактериолога Освальда Эвери в опытах с бактериями убедительнейшим образом продемонстрировали, что именно нуклеиновые кислоты (в данном случае дезоксирибонуклеиновая кислота, ДНК) отвечают за передачу наследственных свойств. Белки были лишены звания „молекул жизни“ и низведены до немного обидного положения „прислуги за всё“. Началась эра молекулярной биологии.
В 1953 году английские учёные Джеймс Уотсон, Френсис Крик и Морис Уилкинс открыли способ укладки ДНК, давший ключ к пониманию принципа передачи генетической информации. Молекула ДНК оказалась очень длинной (по масштабам клетки) двухнитчатой спиралью, закрученной вокруг своей оси. Когда клетке необходимо разделиться, она непосредственно перед этим копирует молекулы ДНК в своих хромосомах. При этом две нити ДНК расходятся, и на каждой из них, как на матрице, собирается дочерняя нить, в точности повторяющая ту, что была соединена с данной нитью в родительской клетке. В итоге появляются две идентичные дочерние хромосомы, которые при делении распределяются по разным клеткам. Так происходит передача наследственных признаков от родителей потомкам у всех клеточных организмов, имеющих ядро.
Итак, если ДНК играет ключевую роль для живого, почему бы не предположить, что именно она была той молекулой, которая и дала начало самой жизни? Если так, то ДНК должна соответствовать „минимальному набору критериев живого“: хранить и передавать информацию о своей структуре и происходящих в ней изменениях в ряду генераций (поколений).
Что же на самом деле умеет ДНК? Опыты Эвери показали, что с помощью ДНК можно передать какое-либо новое, нехарактерное для данного организма свойство. Но как это происходит внутри клетки? Какая информация и каким образом „закодирована“ внутри ДНК? Как она может „считываться“ и распределяться по всей клетке?
Конечно, зная уже достаточно о ключевой роли белков в клетке, учёные с самого начала догадывались, что в ДНК записана информация именно о белках. Основным местом сборки белков служат рибосомы — специально предназначенные для этой цели структуры в цитоплазме клетки. Рибосомы, как было известно, не связываются с ДНК напрямую. Как же информация с ДНК может проникнуть к рибосомам?
Очевидно, для этого необходима какая-то другая молекула — посредник между ДНК и белками. В 60-х годах ХХ века загадка молекулы-посредника была решена. Ею оказалась молекула, родственная ДНК и названная рибонуклеиновой кислотой (РНК).
Обе нуклеиновые кислоты — ДНК и РНК — были открыты швейцарским биохимиком Фридрихом Мишером в 1869 году, задолго до выяснения их роли в передаче наследственной информации. А наиболее полную информацию об их химическом строении получил Фабус Арон Теодор Левин (1869–1940), американский учёный, родившийся в России и получивший образование в Петербурге.
„Несущей конструкцией“ у обеих кислот является так называемый „сахарофосфатный остов“, который у ДНК похож на перила спирально закрученной лестницы. Он состоит из остатков сахаров, соединённых между собой в цепочку с помощью остатков фосфорной кислоты. Именно эта конструкция скрепляет и поддерживает структуру молекулы нуклеиновой кислоты.
К молекулам сахаров остова прикреплены азотистые „основания“, которые расположены как ступени лестницы (внутри от „перил“). Именно благодаря взаимодействиям между атомами водорода, азота и кислорода азотистых оснований одиночные цепочки ДНК могут объединяться в двухцепочечные структуры.
Нуклеиновые кислоты синтезируются в клетке из нуклеотидов — комплексов азотистого основания, сахара и остатков фосфорной кислоты, служащих универсальными блоками для построения ДНК и РНК. Существуют пять видов азотистых оснований — аденин (обозначаемый на схемах буквой А), тимин (Т), гуанин (G), цитозин (C) и урацил (U). Особенностью взаимодействий оснований, благодаря которым они могут формировать двухцепочечные нити, является их строгая специфичность: А может взаимодействовать только с Т, а G — с С (такое точное соответствие оснований и нитей ДНК называют комплементарностью, а сами нити и основания — комплементарными друг другу).
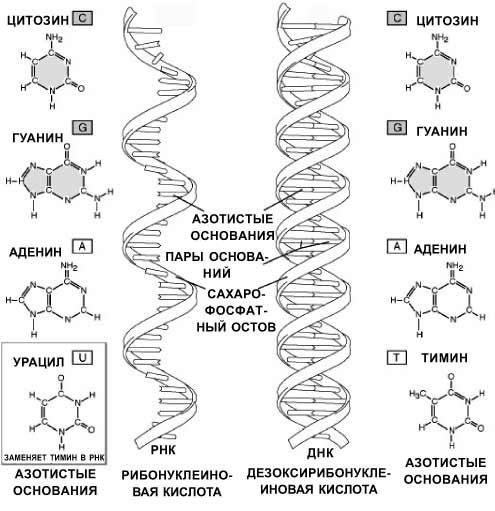 Сравнительная структура РНК и ДНК. Сравнительная структура РНК и ДНК. |
Отличия между РНК и ДНК сводятся к тому, что в состав сахарофосфатного остова РНК входит сахар рибоза, тогда как у ДНК рибоза „теряет“ один атом кислорода и превращается в дезоксирибозу. Кроме того, вместо тимина (Т) в состав РНК входит урацил (U). Урацил отличается от тимина почти так же мало, как рибоза от дезоксирибозы: у него отсутствует лишь боковая метиловая группа (–СН3). Однако такие минимальные отличия в строении РНК и ДНК ведут к существенной разнице в структуре и функциях этих молекул.
Одно из наиболее очевидных различий состоит в том, что РНК большинства организмов, в отличие от двухнитчатой ДНК, существует в виде одной нити. Объясняется это двумя причинами. Во-первых, у всех клеточных организмов отсутствует фермент для катализа реакции образования РНК на матрице РНК. Такой фермент есть лишь у некоторых вирусов, гены которых „записаны“ в виде двухнитчатой РНК. Остальные организмы могут синтезировать молекулы РНК только на ДНК-матрице. Во-вторых, из-за потери метильной группы урацилом связь между ним и аденином получается малоустойчивой, поэтому „удержание“ второй (комплементарной) нити для РНК также является проблемой.
В силу вынужденной однонитчатости РНК, в отличие от ДНК, не закручивается в спираль, а благодаря взаимодействиям внутри одной и той же молекулы образует структуры типа „шпилек“, „головки молотка“, петель, крестов, клубков и прочего.
РНК копируется с ДНК по тем же законам, которые управляют синтезом самой ДНК: каждому основанию ДНК соответствует строго комплементарное основание в строящейся молекуле РНК. Однако, в отличие от копирования ДНК, когда копированию (репликации) подвергается вся молекула, РНК копирует лишь определённые участки на ДНК. В подавляющем большинстве эти участки являются генами, кодирующими белки. Для нашего рассказа важно, что благодаря такому выборочному копированию молекулы РНК всегда короче, а у высших организмов гораздо короче своих „сестёр“ — ДНК. Также важно то, что ДНК в водных растворах более устойчива, чем РНК. Различия во времени их полужизни (то есть времени, за которое разрушается половина данного количества молекул) составляют тысячи раз.
Итак, к середине 60-х годов ХХ века науке стали известны подробности функционирования двух молекул, которые более, чем белки, подходили для роли „молекул первожизни“, — ДНК и РНК. Обе они кодируют генетическую информацию, и обе могут использоваться для её переноса. Но одно дело — возможность нести информацию, и совершенно другое — способность передавать её потомкам самостоятельно, без посторонней помощи. Во всех современных живых системах, от вирусов до высших животных, ДНК или РНК „пользуются услугами“ белков-ферментов для того, чтобы быстро и эффективно, с помощью катализа, передавать свою закодированную информацию в ряду поколений. Ни одна из нуклеиновых кислот в современном мире не может копировать себя самостоятельно. Могла ли такая же кооперация существовать при зарождении жизни на Земле? Как образовалась триада сотрудничающих молекул — ДНК, РНК и белков, на которой построена вся современная жизнь? Кто и почему мог стать „прародителем“ этих трёх „молекулярных китов“?
 2015-05-10
2015-05-10 744
744








