Вариант 1
Исследована кинетика действия глюкозо-6-фосфатдегидрогеназы азотфиксирующих бактерий Azotobacter beijerinckii.
глюкозо-6-фосфат + НАДФ+ ® глюконат-6-фосфат + НАДФН + Н+
Получены приведенные ниже данные о зависимости начальной скорости реакции от концентрации глюкозо-6-фосфата
| Концентрация Глюкозо-6-фосфат, мМ | Начальная скорость восстановления НАДФ+, нмоль/мин |
| 0,375 | 6,65 |
| 0,5 | 9,25 |
| 0,625 | 10,95 |
| 0,75 | 13,09 |
| 0,875 | 15,45 |
| 17,84 | |
| 1,25 | 20,69 |
| 1,5 | 23,80 |
| 29,24 | |
| 2,5 | 35,08 |
Найдите константу Михаэлиса и максимальную скорость реакции методами Лайнуивера-Бэрка, Эди-Хофсти и Хейнса. Сравните полученные результаты.
Вариант 2
Исследовали люциферазную систему ракообразного Cypridina при температуре 15оС. Начальные скорости реакции определяли, регистрируя количество света, испускаемого в единицу времени (мин) с помощью фотоэлемента. Результаты приведены в таблице:
| Количество добавляемого раствора люциферина на 20 мл реакционной смеси, мл | Нач скорость мВ/мин |
| 0,04 | |
| 0,06 | |
| 0,08 | |
| 0,1 | |
| 0,2 | |
| 0,4 | |
| 0,9 |
Концентрация люциферина в добавляемом растворе 8·10-5 М. Найти константу Михаэлиса и максимальную скорость реакции методами Лайнуивера-Бэрка, Эди-Хофсти и Хейнса. Сравнить полученные результаты.
Вариант 3
Известно, что D-сериндегидратаза из Neuruspora crassaиспользует в качестве кофермента пиридоксальфосфат. Фермент катализирует реакцию: СН2(ОН)СН(NH2)COOH ®CH3COCOOH+NH3
При исследовании насыщения фермента пиридоксальфосфатом были получены следующие данные:
| Скорость образования пировиноградной к-ты, мкмоль/20 мин | 0,15 | 0,2 | 0,275 | 0,315 | 0,34 | 0,35 | 0,36 |
| Концентрация пиридоксальфосфата, 10-5 М | 0,2 | 0,4 | 0,85 | 1,25 | 1,7 | 2,0 | 8,0 |
Найти константу Михаэлиса и максимальную скорость реакции методами Лайнуивера-Бэрка, Эди-Хофсти и Хейнса. Сравнить полученные результаты.
Вариант 4
Начальная скорость выделения O2 при действии фермента на субстрат была измерена для ряда концентраций субстрата:
| [S], моль/л | 0,050 | 0,017 | 0,010 | 0,005 | 0,002 |
| V, мм3/мин | 16,6 | 12,4 | 10,1 | 6,6 | 3,3 |
Найти константу Михаэлиса и максимальную скорость реакции методами Лайнуивера-Бэрка, Эди-Хофсти и Хейнса. Сравните полученные результаты.
Вариант 5
Процесс декарбоксилирования глиоксилата митохондриями исследовали по скорости выделения СО2 для различных концентраций глиоксилата. Найти константу Михаэлиса и максимальную скорость исследуемого процесса методами Лайнуивера-Бэрка, Эди-Хофсти и Хейнса. Сравните полученные результаты.
| Концентрация глиоксилата, мМ | Скорость выделения СО2 (усл.ед.) |
| 2,5 | |
| 0,75 | 2,44 |
| 0,6 | 2,08 |
| 0,5 | 1,89 |
| 0,4 | 1,67 |
| 0,33 | 1,39 |
| 0,25 | 1,02 |
Вариант 6
Метионин образуется при биосинтезе (Escherichia coli) в результате ферментативного метиллрования гомоцистеина 5-метилтетрагидроптероилтриглутаматом. Образование метионина регистрировали микробиологическим методом. Были получены следующие результаты:
| Триглутамат, мкмоль/л | Кол-во образовавшегося метионина, нмоль |
| 12,5 | |
| 16,7 | |
Найти константу Михаэлиса и максимальную скорость реакции методами Лайнуивера-Бэрка, Эди-Хофсти и Хейнса. Сравните полученные результаты.
Вариант 7
При изучении зависимости скорости реакции от концентрации субстрата были получены след. данные. Субстратом служил фенолфталеинглюкуронид; скорость реакции выражали в микрограммах фенолфталеина, освобождаемого за 60 минут при 37оС. Найти константу Михаэлиса и максимальную скорость реакции методами Лайнуивера-Бэрка, Эди-Хофсти и Хейнса. Сравните полученные результаты.
| Концентрация субстрата, мМ | Скорость реакции |
| 43,6 | |
| 50,4 | |
| 56,5 | |
| 62,1 |
Вариант 8
Начальная скорость окисления сукцината натрия в фумарат натрия под действием фермента сукциноксидазы была измерена для ряда концентраций субстрата:
| [S], моль/л | 0,01 | 0,002 | 0,001 | 0,0005 | 0,00033 |
| V·106, моль/(л·с) | 1,17 | 0,99 | 0,79 | 0,62 | 0,50 |
Определите константу Михаэлиса и максимальную скорость данной реакции методами Лайнуивера-Бэрка, Эди-Хофсти и Хейнса. Сравните полученные результаты
Вариант 9
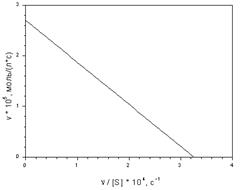 Найдите константу Михаэлиса и максимальную скорость каталитического разложения гидроперекиси тетралина по следующим кинетическим данным:
Найдите константу Михаэлиса и максимальную скорость каталитического разложения гидроперекиси тетралина по следующим кинетическим данным:
Используя уравнение Михаэлиса-Ментен, найдите значения концентрации субстрата для нескольких значений скорости реакции. По полученным данным рассчитайте максимальную скорость реакции и константу Михаэлиса методами Лайнуивера-Бэрка и Хейнса. Сравните полученные результаты.
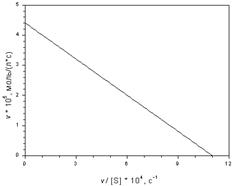 Примечание: Для нахождения концентраций субстрата выбрать несколько значений скорости по предложенному графику и записать их в виде массива. Из уравнения Михаэлиса-Ментен выразить значение S через найденные величины V, Km и Vmax. Поскольку полученная формула предполагает действия с векторами, над выражением необходимо поставить знак вектора (панель инструментов Matrix, кнопка с изображением
Примечание: Для нахождения концентраций субстрата выбрать несколько значений скорости по предложенному графику и записать их в виде массива. Из уравнения Михаэлиса-Ментен выразить значение S через найденные величины V, Km и Vmax. Поскольку полученная формула предполагает действия с векторами, над выражением необходимо поставить знак вектора (панель инструментов Matrix, кнопка с изображением 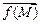 ).
).
Вариант 10.
Найдите константу Михаэлиса и максимальную скорость каталитического окисления циклогексена трет-бутилпероксидом по следующим кинетическим данным:
Используя уравнение Михаэлиса-Ментен, найдите значения концентрации субстрата для нескольких значений скорости реакции. По полученным данным рассчитайте максимальную скорость реакции и константу Михаэлиса методами Лайнуивера-Бэрка и Хейнса. Сравните полученные результаты.
 2015-05-13
2015-05-13 1158
1158








