|
Молярной теплоемкостью вещества называется энергия, необходимая для нагревания 1 моля на один градус.
Величина теплоемкости газа зависит от способа его нагревания. Как известно из термодинамики, Cv - молярная теплоемкость идеального газа при постоянном объеме и Cp – при постоянном давлении соответственно равны:
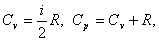
где
R – универсальная газовая постоянная,
i – число степеней свободы молекулы.
Отношение  - называется коэффициентом Пуассона. - называется коэффициентом Пуассона.
Экспериментальное устройство состоит из стеклянного баллона А, соединенного с жидкостным манометром М и насосом (см. рисунок).

Посредством крана К1 система может быть изолирована от атмосферы. Пусть в системе первоначально было Рa – атмосферное давление. В баллон А накачивают небольшое количество воздуха и закрывают кран К2. При плохом обмене теплом с окружающей средой температура воздуха в баллоне несколько повышается. Через некоторое время  воздух в баллоне принимает температуру окружающей среды. При этом разность уровней в манометре становится h1. Это состояние воздуха назовем первым. Его параметры: воздух в баллоне принимает температуру окружающей среды. При этом разность уровней в манометре становится h1. Это состояние воздуха назовем первым. Его параметры:
- давление -

- удельный объем -
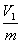
- температура – Т1
Кратковременным поворотом крана К1 систему соединяют с атмосферой. При этом происходит быстрое расширение воздуха. Давление в системе становится равным атмосферному, а температура из-за быстрого расширения несколько понижается.
Параметры второго состояния:
- давление -
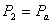
- удельный объем -

- температура -

Переход от первого состояния ко второму описывается уравнением Пуассона:
 (1) (1)
или
 (2) (2)
Как только давление в системе станет равным атмосферному, кран К1 закрывают. После этого, охладившийся при расширении воздух за время  нагревается до температуры окружающей среды и давление возрастает. нагревается до температуры окружающей среды и давление возрастает.
Параметры третьего состояния:
- давление -
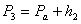
- удельный объем -

- температура -
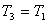
Второе и третье состояния связаны уравнением изохоры:
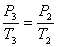 (3) (3)
из (2) и (3) получаем:
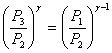 (4) (4)
или
 (5) (5)
Разложив это выражение по формуле бинома Ньютона и ограничившись членами первого порядка, получим:
 (6) (6)
Выполнение работы
Определяют времена  и и  установления термодинамического равновесия. Для этого в баллон нагнетают воздух до давления, превышающего атмосферное на 7-8 см высоты столба жидкости в манометре и, измеряя давление в системе через 10-15 сек, строят график установления термодинамического равновесия. Для этого в баллон нагнетают воздух до давления, превышающего атмосферное на 7-8 см высоты столба жидкости в манометре и, измеряя давление в системе через 10-15 сек, строят график
 (7) (7)
Кратковременным поворотом крана К1 систему соединяют с атмосферой. Кран К1 закрывают, когда уровни жидкости в манометре станут одинаковыми.
Строят график
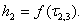 (8) (8)
- Из графиков (7) и (8) определяют времена
 и и  установления термодинамического равновесия. установления термодинамического равновесия.
- Измеряют h1 и h2.
- Вычисляют
 . .
В силу ряда причин результаты отдельных экспериментов отличаются друг от друга. Поэтому опыт повторяют 10-15 раз.
Из полученных результатов находят среднее значение 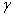 . .
| 

 (2)
(2)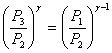 (4)
(4) (5)
(5)








