Рассчитайте активность ионов в 0,01 М растворе СаСl2.
СаCl2 ® Ca2+ + 2Cl-
С, моль/л: 0,01 0,012×0,01
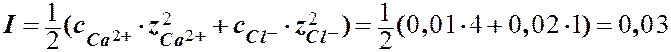 | |||
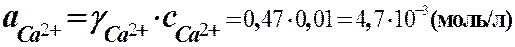 |
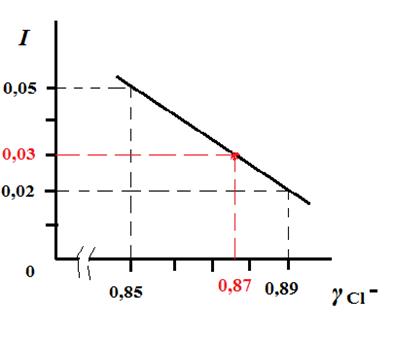
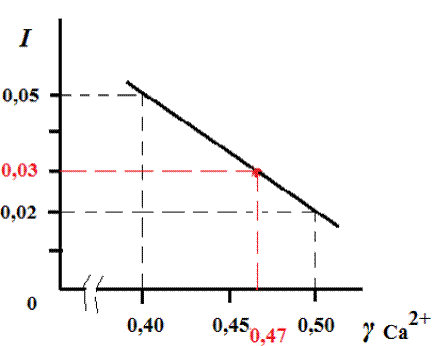
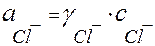 = 0,87×0,02 = 1,74×10-2 (моль/л)
= 0,87×0,02 = 1,74×10-2 (моль/л)
Расчет рН сильных кислот и оснований
а) для кислот:
I р-ра = 0,5 × å(сi × z 2 i) Þ gН+ (по таблице или формуле)
Þ а Н + = gН+ × с Н+ Þ рН = -lg а Н +
б) для оснований:
I р-ра = 0,5 × å(сi × z 2 i) ÞgOН- (по таблице или формуле)Þ а ОН - = gОН-× с ОН-Þ рН = 14 + lg а ОН-
рН = 14 - рОН =14 + lg а ОН - = 14 + lg gОН-. с ОН-
ЗАДАЧА
Рассчитайте рН 0,05 М раствора НСN.
Решение.
НСN 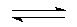 Н+ + СN-
Н+ + СN-
слабая кислота, с о = 0,05 моль/л, К Д= 7,9×10-10 (из таблицы)
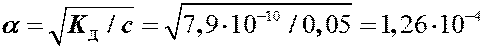 |
a < 0,07 Þ расчет по упрощенной формуле:
с H+ = aсо = 1,26×10-4×0,05 = 6,3×10-6 моль/л
рН = ‑lg с H+ = - lg 6,3×10-6 = 5,18.
ЗАДАЧА
Рассчитайте концентрацию азотистой кислоты НNО2 в растворе с рН = 2,7.
 2015-05-26
2015-05-26 690
690








