Масса 1л раствора равна:
m р-ра = r р-ра V р-ра = 1,18×1000 = 1180 г.
В 1 л р-ра:
m (H3PO4) = (m р-ра ∙ w)/100% = (1180×30)/100 = 354 г.
M (H3PO4) = 98 г/моль.
v (H3PO4)= m (H3PO4)/ M (H3PO4) =354/98 = 3,61 моль.
Þ сМ = 3,61 моль/л, (3,61 М H3PO4).
Нормальность -?
Э(H3PO4) =1/3 H3PО4, fэ (H3PO4) = 1/3
в 1 моле H3PО4 содержится 3 моль-эквивалента
Þ в 1 л раствора 3,61×3 = 10,83 моль -экв Н3РО4.

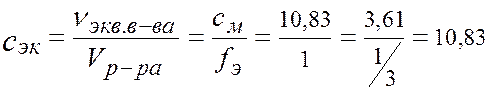 моль/л
моль/л
с эк = 10,83 моль/л, (10,83 н H3PO4).
Титр -?
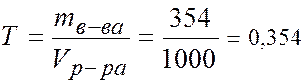 г/мл
г/мл
Т = 0,354 г/мл/
Моляльность -?
В 100 г раствора: 30 г Н3РО4 и 70 г Н2О.
В 1000 г Н2О:
m (H3PO4)= (1000×30)/70 = 428,5 г.
v (H3PO4) = m (H3PO4)/ M (H3PO4) = 428,5/98 = 4,37 моля.
Þ сm = 4,37 моль/1000 г Н2О.
Молярная доля -?
В 1л раствора:
m (H2O) = 1180 – 354 =826 г.
v (H2O) = m (H2O)/ M (H2O) = 826/18 = 45,89 молей.
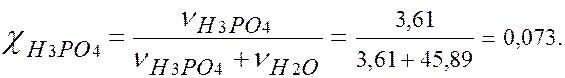
χ (H3PO4 ) = 0,073.
ЗАДАЧА
Р н.п. чистого ацетона(СО(СН3)2) при 20º С равно 23940 Па.
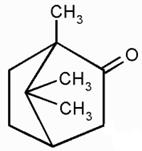 Р н.п. ацетона над раствором, содержащем 5 г камфоры на 200 г ацетона, при той же Т равно 23710 Па. Определите молекулярную массу камфоры.
Р н.п. ацетона над раствором, содержащем 5 г камфоры на 200 г ацетона, при той же Т равно 23710 Па. Определите молекулярную массу камфоры.
 2015-05-26
2015-05-26 709
709








