По определению: b = cГ / c 0= [OH]/ c 0 Þ[OH] = b×c 0
рН = 14 – рОН = 14 + lg [OH] = 14 + lg (b×c 0)
а) b - по строгой формуле 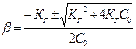
б) b - по приближенной формуле (если К Г<10-4):
b ≈ 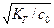 =
= 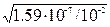 = 4×10-3 << 1 Þ расчет по приближенной формуле правомерен.
= 4×10-3 << 1 Þ расчет по приближенной формуле правомерен.
[OH] = b×c 0 = 4×10-3×10-2 = 4×10-5 рН = 14 + lg [OH] =14 - 4,4 = 9,6
КГ = КВ/КД кислоты Þ 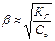 Þ с ОН- = b×со Þ рН=14+ lg(
Þ с ОН- = b×со Þ рН=14+ lg( 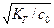 )
)
Аналогично:
Расчет рН растворов солей с гидролизом по катиону
КГ = КВ/КД основания Þ 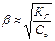 Þ с Н+ = b×со Þ рН= - lg(
Þ с Н+ = b×со Þ рН= - lg( 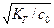 )
)
Расчет рН, если гидролиз идет по катиону и аниону
(концентрация соли не влияет на b)
КГ = КВ/ (КД кислоты КД основания) Þ 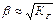 Þ
Þ
с Н+ = 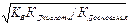 Þ рН = 0,5[- lgK В - lgК Д(к-ты) + lgК Д(осн)] =0,5[рКВ +р К Д(к-ты) - р К Д(осн)]
Þ рН = 0,5[- lgK В - lgК Д(к-ты) + lgК Д(осн)] =0,5[рКВ +р К Д(к-ты) - р К Д(осн)]
(- lgK В = р K В при 250 С р K В = 14)
 2015-05-26
2015-05-26 867
867








