Определить С Р(MgF2) в растворе, в котором g(Mg2+) = 0,7, g(F-) = 0,96
Решение:
MgF2 (т) Û Mg2+ (нас.р-р) + 2F-(нас.р-р)
ПР(MgF2) = 4×10-9 = 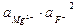
сР = 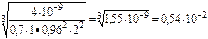 моль/л
моль/л
Растворимость С Р зависит от:
· ионной силы раствора: при ↑ ионной силы раствора (I) gi ↓ и с Р ↑
(чтобы при Т=const ПР =const);
· от введения одноименного к имеющимся иона: равновесие смещается влево и с Р ↓. MgF2 Û Mg2+ (нас.р-р) + 2F-(нас.р-р)
NaF → Na+ (р-р) + F-(р-р)
На этом явлении основан метод осаждения (растворимость СаСО3 и МgСО3 падает 
 при введении в раствор хорошо растворимых К2СО3 или Nа2СО3 Þ ионы жесткости Са2+ и Мg2+ удаляются из раствора).
при введении в раствор хорошо растворимых К2СО3 или Nа2СО3 Þ ионы жесткости Са2+ и Мg2+ удаляются из раствора).
· от комплексообразования: (повышение с р при образовании комплексов)
KCl + AgNO3 = KNO3 + AgCl↓
AgCl↓ + KCl = K[AgCl2]- хорошо растворим
 2015-05-26
2015-05-26 271
271








