Для выполнения работы методом последовательного разведения готовится ряд растворов сильной кислоты (хлороводородной, азотной, серной, или другой по указанию преподавателя) различной концентрации: 0,2М; 0,1М; 0,05М; 0,01М; 0,005М.
Исходным раствором служит 2М раствор электролита (либо более концентрированный).
Растворы готовят в мерных колбах на 100мл.
Для получения более точных результатов концентрации приготовленных растворов устанавливают кислотно-основным титрованием (титруют раствором щелочи соответствующей концентрации).
Результаты титрования заносят в таблицу 3.
Таблица 3 − Результаты титрования
| № п/п | Заданная концен-трация раствора, моль/л | Концен- трация щелочи, моль/л | Объем пробы, мл | Объем щелочи, пошедший на титрование | Средний объем щелочи, мл | Точная концен- трация кислоты, моль/л |
Затем измеряют рН приготовленных растворов.
Рассчитывают ан+ = 10–рН.
Экспериментальное значение коэффициента активности определяют из отношения γ Н+ = aH+./СН+.
Расчетное значение коэффициента активности определяют из уравнения Дебая-Хюккеля первого приближения, если I < 0,01m:
lgγi = − 0,51 zi2 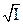
Если 0,01m <I < 0,1m, то коэффициента активности определяют из уравнения Дебая-Хюккеля второго приближения:
lgγi = – 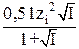 .
.
Результаты измерений pH и расчетов оформляют в виде таблицы 4.
Таблица 4 – Экспериментальные результаты по изучению сильного электролита
| № п/п | Концентрация раствора, моль/л | рН | аH+, моль/л | I, моль/л | γi ЭКСП | γi РАСЧ |
По результатам расчетов строят два графика на одной координатной плоскости (рис. 3): зависимость γi ЭКСП и γi РАСЧ от концентрации сильной кислоты γi ЭКСП = f(CM) и γi РАСЧ = f(CM).
По результатам расчетов необходимо сделать выводы о применимости теории Дебая-Хюккеля. С помощью построенных графиков необходимо установить характер зависимости коэффициента активности иона водорода от концентрации кислоты.
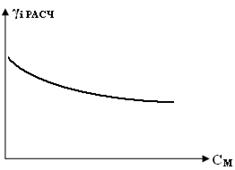
Рис.3 – Зависимость коэффициента активности иона водорода γi РАСЧ от концентрации раствора кислоты
 2015-05-26
2015-05-26 953
953








