В качестве количественной меры способности раствора электролита проводить электрический ток используют обычно удельную электропроводность (æС) – электропроводность раствора электролита, заключенного между плоскими электродами площадью 1м2, находящимися на расстоянии 1м, т.е. электропроводность 1м3 раствора электролита.
Величина удельной электропроводности электролита зависит от ряда факторов: природы электролита, температуры, концентрации раствора. Удельная электропроводность растворов электролитов с увеличением температуры возрастает, что вызвано увеличением скорости движения ионов за счет понижения вязкости раствора.
С увеличением концентрации удельная электропроводность растворов сначала возрастает, достигая некоторого максимального значения, затем начинает уменьшаться. Эта зависимость очень чётко выражена для сильных электролитов и значительно хуже для слабых (рис. 4). В разбавленных растворах удельная электропроводность раствора сильного электролита растет почти пропорционально концентрации, т.е. числу носителей заряда – ионов в единице объема раствора. С ростом концентрации усиливается взаимодействие ионов, что уменьшает скорость их движения и электропроводность раствора.
Для слабых электролитов наличие максимума на кривой обусловлено тем, что с ростом концентрации уменьшается степень диссоциации, и при достижении определенной концентрации число ионов в растворе начинает увеличиваться медленнее, чем концентрация электролита.
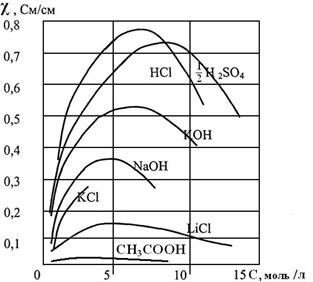
Рис. 4 – Зависимость удельной электропроводности
растворов электролитов от их концентрации
 2015-05-26
2015-05-26 1311
1311
