В начале 1970-х годов, используя нервно-мышечный синапс лягушки, Катц и Миледи предприняли оригинальные эксперименты, в которых метод внутриклеточной микроэлектродной регистрации использовался для изучения характеристик «шумов», продуцируемых медиатором ацетилхолином (АХ). В таком синапсе АХ, освобождающийся из моторного нервного окончания, открывает хемовоз-будимые ионные каналы постсинаптической мембраны. Вход катионов в волокно через открытые ионные каналы вызывает деполяризацию мембраны (глава 9). Когда Катц и Миледи локально апплицировали экзогенный АХ на область синапса, они обнаружили, что вызванная деполяризация сопровождалась электрическим «шумом». Во время стабильной деполяризации быстрые колебания потенциала были гораздо больше колебаний изолинии в покое. Они предположили, что возрастание электрического шума в присутствии АХ было связано с хаотичным открытием и закрытием АХ-активируемых ионных каналов. Иными словами, аппликация АХ приводила к открытию большого числа ионных каналов, и число это случайно колебалось в зависимости от числа взаимодействий АХ с рецепторами.
Используя известную из физики технику анализа шума, Катц н Миледи смогли получить информацию о среднестатистическом поведении отдельного ионного канала, активируемого АХ. Позднее подобные эксперименты были проведены на том же объекте Anderson и Stevens3). В отличие от предшественников, эти исследователи измеряли мембранный ток, вызванный АХ, что позволило установить величину и продолжительность ионных токов через одиночный канал (рис. 2.5В).
Принципы анализа шума достаточно просты: во-первых, если токи одиночного канала являются большими, суммарный шум также будет большим. Во-вторых, ионные каналы, открывающиеся на относительно длительное время, будут продуцировать низкочастотный шум; наоборот, каналы, открывающиеся на короткое время, будут продуцировать высокочастотный шум. Исследование амплитудно-временных характеристик шумов, ак-
Раздел II. Передача информации в нервной системе
 |
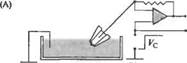
| Рис.2.5. Внутриклеточное отведение электрического «шума», производимого функционированием ионных каналов. (А) Схема установки для регистрации мембранного потенциала. (В) Внутриклеточная регистрация эффекта аце-тилхолина. (С) При большем усилении виден ацегилхолиноеый «шум». Fig.2.5. Intracel ular Recording of Channel Noise. (A) Arrangement for recording membrane potentials of muscle fibers with a microelectrode. The electrode is connected to a preamplifier, and the signals are displayed on an oscilloscope or computer screen. Penetration of the electrode into a fiber is marked by the sudden appearance of the resting potential (downward deflection on the screen). After penetration, changes in potential due to channel activation can be measured. (B) Intracellular records of the effect of acetylcholine (ACh). In this experiment additional circuitry was used to record membrane current (rather than membrane potential). At rest (upper trace), there is no current across the membrane; application of ACh produces about 130 nA of inward current (lower trace). (C) Traces in В shown at greater amplification. The baseline shows little fluctuation at rest; the inward current produced by ACh shows relatively large fluctuations ("noise"), due to random opening and closing of ACh-activated channels. Analysis of the increased noise yields values for the single-channel current and the mean open time of the channels. (B and С after Anderson and Stevens, 1973.) |
| Preamplifier |
(A) Mlcroelectrode
| В | |||
| Muscle chamber B) | Oscilloscope Rest | ||
| 1S -100 | - | ACh I | |
| <-> -200 | - | 1 1 1 1 | |
0 0.1 0.2 0 3 04 0.5 0.6
| (С) |
Rest

 0 0.1 0.2 0.3 0.4 0.5 0.6 Time (s)
0 0.1 0.2 0.3 0.4 0.5 0.6 Time (s)
| Проводимость каналов Кинетическое поведение канала, то есть время его нахождения в закрытом и открытом состояниях, может предоставить информацию о механизмах открытия и закрытия канала, а также о константах скоростей этих процессов. С другой стороны, величина тока, проходящего через ионный канал, является прямым отражением того, как быстро проникающие ионы движутся через канал. Ток ионов зависит не только от свойств канала, но также от трансмембранного потенциала. Пример такого рода показан на рис. 2.6. На этом рисунке изображен фрагмент мембраны, который содержит один спонтанно активный ионный канал, проницаемый для калия. Растворы, как в пипетке, так и в ванночке для объекта, содержат одинаковую (150 ммоль) концентрацию ионов калия. Ионы калия через открытый канал могут двигаться в обоих направлениях. Однако поскольку концентрации ионов по обе стороны мембраны идентичны, а трансмембранный потенциал отсутствует, то нет никакого движения ионов ни в одном |
тивированных АХ в нервно-мышечном синапсе, показало, что через одиночный открытый ионный канал проходит около 10 миллионов ионов в секунду. Кроме того, выяснилось, что значение среднего открытого времени (т) ионного канала составляет от 1 до 2 мс.
Несмотря на широкое вытеснение пэтч-кламп методом, анализ шума до сих пор используется для изучения ионных каналов в клетках, которые не поддаются исследованию с помощью пэтч-клампа, например, в некоторых областях центральной нервной системы8). Кроме того, анализ шума является сравнительно быстрым методом для получения информации о свойствах большой популяции каналов и используется в комбинации с пэтч-кламп регистрацией от целой клетки для идентификации типов каналов. Тем не менее, надо понимать, что с помощью анализа шума невозможно получить детальную информацию о поведении одиночного канала, особенно в каналах со сложной кинетикой или при наличии нескольких уровней проводимости канала.
Глава 2. Ионные каналы и нейранальная сигнализация

|
(В)
Г Out
MV

 -lL In
-lL In
 | ||
 |
| - In |
| - Out |
Рис. 2.6. Влияние потенциала на ток
| (С) |
через одиночный калиевый канал
в симметричном растворе ионов калия
по обе стороны мембраны. (А) Схема
установки. (B-D) Примеры токов через
одиночные ионные каналы при разных о _2
уровнях мембранного потенциала. (Е)
Ток через калиевый канал как функция
мембранного потенциала.
Fig. 2.6. Effect of Potential on Currents (D)? 2
through a single, spontaneously active 5
potassium channel in an outside-out g
patch, with 150 mM potassium in both ^ _,
| (E) |
the electrode and the bathing solu
tion. (A) The recording system. The
output from the patch clamp amplifier
is proportional to the current across the
patch. The potential across the patch
is equal to the potential (VC) applied
to the input of the amplifier as shown.
Positive charge flowing out of the elec
trode is defined as positive current. (B)
When no potential is applied to the
patch, no channel currents are seen be- <
cause there is no net flux of potassium
through the channels. (C) Application g,_
of +20 mV to the electrode results g -40
in an outward current (upward deflec
tions) of about 2 pA through the chan- J
nels. (D) A -20 mV potential results
in inward channel currents (downward
deflections) of the same amplitude as
in С. (Е) Channel currents as a function
of applied voltage. The slope of the line
is the channel conductance (7). In this
case, 7 = 110 pS (picosiemens).
+20 mV
 -20 mV
-20 mV
ггиппгыпгг
In
 2015-05-30
2015-05-30 628
628








