Ежегодно в мире сжигается 10 млрд.тонн условного топлива, причем делается это очень расточительно. Коэффициент полезного действия тепловых электрических станций составляет лишь 20%, дизель генераторов – 37%, газовых турбин – 50%, топливных элементов – 60%. Сочетание их с газовой турбиной позволяет поднять к.п.д. до 75%.
Топливные элементы – это химические источники электрической энергии, предназначенные для превращения в электрическую энергию химической энергии, получаемой от сгорания топлива.
Превращать энергию сжигания топлива в электрическую предложил Яблочков П.Н. в 1880 г.
Водородно-кислородный элемент предложен в 1939 г. Грове, элемент работал при комнатной температуре, атмосферном давлении, обеспечивал очень низкие токи, сильно поляризовался, имел низкие к.п.д.
При переходе к воздушному электроду вместо кислородного, э.д.с. снижается. Подбор материалов, снижающих перенапряжение выделения кислорода и водорода позволил рекомендовать для отрицательных электродов Pd, Pd- или платинированный графит, для положительных порошки Ag и Ni в смеси с активным углем. Повышение температуры и давления позволяет увеличить плотности тока.
В 1959 г. Бэкон, Кембридж, создал батарею из кислородно-водородных элементов мощностью 5 кВт.
Под топливными элементами (ТЭ) подразумевают такие источники тока, в которых активные вещества хранятся отдельно, происходит постоянная подача их из внешних хранилищ внутрь источника тока, в зону электрохимической реакции, и постоянный отвод продуктов реакции из источника тока. Электроды выполняют роль катализаторов электрохимических реакций и токоотводов. Заметим, что электроды при этом не расходуются и, в принципе, могли бы работать неограниченное время, если бы не различные привходящие обстоятельства.
Классифицируются ТЭ чаще всего по температурному режиму их работы. Так, различают низкотемпературные (до 100°С), среднетемпературные (до 300°С) и высокотемпературные ТЭ (выше 500°С). Кроме того, имеется группа регенеративных ТЭ, которые могут быть и низкотемпературными, и высокотемпературными.
Водородно-кислородные низкотемпературные топливные элементы (НТТЭ) наиболее разработаны, они бывают со щелочным, кислотным и ионообменным электролитами.
Работа НТТЭ со щелочным электролитом описывается уравнениями реакций:
на аноде
2Н2 + 4ОН- - 4е =4Н2О (6.23)
на катоде
O2 +2H2O + 4e = 4OH-
He + O2 =2Н2О
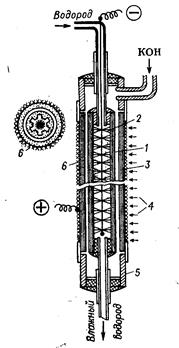
Рис. 179. Водородно-кислородный элемент с пористыми цилиндрическими угольными электродами: 1—полый цилиндрический водородный электрод; 2 — токоотвод водородного электрода; 3—полый цилиндрический кислородный (воздушный) электрод; 4—подвод воздуха к электроду; 5—пластмассовые муфты; 6—токоотвод кислородного электрода.
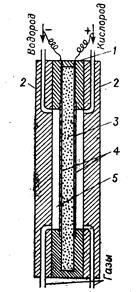
Рис. 180. Схема водородно-кислородного элемента с ионообменной мембраной:
1 — уплотняющие прокладки; 2 — стенки газовых камер; 3—ионообменная мембрана; 4—электроды; 5—газовые камеры.
Основная задача при разработке этих и других типов ТЭ с газообразными активными веществами состоит в создании устойчивой границы соприкосновения трех фаз (газовой, жидкой и твердой), на которой совершается основной токообразующий процесс. Такая граница создается конструированием электродов с заданной пористостью. Положение границы раздела регулируют либо внешним давлением газа (в элементе Бэкона), либо капиллярным давлением электролита (в элементе Юсти).
Водородный электрод получают спеканием карбонильного никелевого порошка; в качестве катализатора используют добавку высокоактивного (рэнеевского) никеля. Для этого к карбонильному никелю добавляют мелкораздробленный сплав никеля с алюминием, прессуют и спекают в водородной атмосфере. Затем алюминий выщелачивают, обрабатывая растворами щелочи. Положительный (кислородный) электрод делают тоже из никеля, но катализатором служит дисперсное (скелетное) серебро. Электроды применяют двухслойные, причем слой, прилегающий к газовой фазе, должен быть крупнопористым, а слой, соприкасающийся с электролитом, — мелкопористым. Давление газа в электроде выбирают с таким расчетом, чтобы электролит был вытеснен из крупнопористого слоя, тогда как мелкопористый слой, благодаря капиллярным силам, оставался бы пропитанным электролитом. Этот слой (его называют запорным) не позволяет газу переходить в виде пузырьков в электролит.
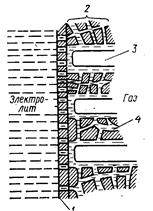
Рис. 1.40. Схема распределения жидкости и газа в бипористом газожидкостном электроде:
1 — запорный слой; 2 — активный слой; 3 — поры, заполненные газом; 4 — поры, заполненные жидкостью.
Рассматриваемые элементы допускают плотности тока 100 — 200 мА/см2, работают на протяжении сотен и тысяч часов и имеют удельную мощность порядка 50 Вт на 1 кг массы батареи. Электролитом в указанном ТЭ служит 30% раствор КОН.
Теоретическое значение удельной энергии кислородно-водородного НТТЭ при 25°С составляет 3650 Вт×ч/кг активных веществ. Практически больше 1000— 1500 Вт×ч/кг получить не удается. Это обусловлено тем, что масса баллонов для хранения водорода в 50 -100 раз больше массы газа.
При хранении водорода в сжиженном состоянии с применением слоистой вакуумной тепловой изоляции масса тары только в несколько раз превышает массу газа.
Практическое применение находят также НТТЭ с жидким (растворенным) топливом (спирты, гидразин, бензин, мазут). Особенно большое внимание уделяется гидразин-кислородному ТЭ со щелочным электролитом. В присутствии таких катализаторов, как палладий, платина или никель, гидразин разлагается на водород и азот по уравнению
N2H4 =N2 + 2H2 (6.24)
Образующийся при этом водород используется как топливо для ТЭ. В США построены и эксплуатируются опытные образцы таких батарей. Преимущество этих батарей заключается в удобстве хранения и транспортирования гидразина, не требующего применения высоких давлений или низких температур, недостаток — высокая токсичность гидразина и его паров.
Среднетемпературные топливные элементы (СТТЭ) представляют собой водородно-кислородные ТЭ, работающие при 250—300°С и при давлении газов до 6 МПа. Электролитом служит 85% раствор щелочи, находящийся при рабочей температуре в жидком состоянии. Электроды никелевые, без катализаторов. Элемент имеет пологие вольт-амперные характеристики: с увеличением плотности тока от 100 до 200 мА/см2 напряжение элемента падает от 1,05 до 0,9 В.
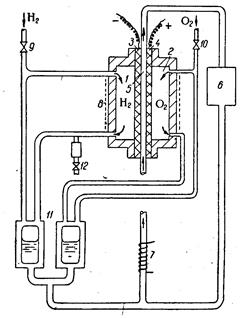
Схема установки «Гидрокс»: 1- водородная камера, 2 – кислородная камера, 3 – водородный электрод (анод), 4 – кислородный электрод (катод), 5 – электролит, 6 – резервуар с электролитом, 7 – нагреватель для циркуляции электролита, 8 – обогрев элемента, 9 – штуцер подачи водорода, 10 – штуцер подачи кислорода, 11 – регулятор давления газа и электролита, 12 – конденсатор и дроссель для удаления воды.
У камер 1,2 стенки обращенные друг к другу сделаны из микропористых никелевых дисков диаметром 127 мм, толщиной 4 мм. Изготавливают их металлокерамическим способом. Диаметр пор к газу 30 мк, к электролиту 15 мк.
Электролит 27% КОН, температура 200-240°С, Р=40-56 атм. Давление газа на 0,1 атм больше давления электролита. В результате электролит не проникает в более крупные поры (30 мк) и они открыты для адсорбции газов. В то же время при DР=0,1 атм газ не может выдавить жидкость из пор 15 мк.
Т.о. создается устойчивая 3-фазная граница газ – электролит -металлический электрод для реализации электрохимических реакций.
При 240°С и 56, 2 атм. Элемент «Гидрокс» имел следующие показатели:
Нагрузка, А/см2 0 0,162 0,413 1,076
Напряжение, В 1,05 0,9 0,8 0,6
К.п.д.,% - 77 68 51,5
К числу СТТЭ относится также ТЭ, в котором в качестве электролита применен 85% раствор ортофосфорной кислоты, адсорбированный пористой прокладкой и пористыми платиновыми электродами. Рабочая температура — от 150 до 200 °С. В качестве окислителя применяется кислород, а в качестве топлива — водород, пары спирта и некоторые углеводороды.
Для практики более интересны воздушно-угольные или воздушно-водородоуглеродные топливные элементы, но они реализуются только при повышенных температурах.
В 1937 г. Бауру предложил воздушно-угольные ТЭ с твердым электролитом, работающие при1000-2000°С.
Электролит получен спеканием СеО2 и WO3 при 1100°С, либо прокаливанием Fe2O3(магнетит) (воздушный электрод). В элементе реализуется реакция
2С + О2 =2СО
Кислород в ионизированном состоянии переносится через твердый электролит к углю
Процессы на электродах:
- С + О2—2е = СО
+ 1/2О2 + 2 е = О2-.
Е = 0,7В; I = 1,5-2,0 А/1 л объема.
Предложенный О.К.Давтяном ТЭ использовал энергию реакции
2СО + О2 =2СО2.
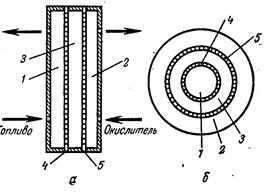
Рис. 1-18. Схема устройства топливного элемента: а—элемент с плоскими электродами; б—элемент с трубчатыми электродами; 1—газовая камера топлива; 2—газовая камера окислителя; 3—электролит; 4—диффузионный анод; 5—диффузионный катод.
1 - воздушный электрод, 2 – топливный электрод (СО), 3 – твердый электролит с кислородной проводимостью, 4 – воздушная камера, 5 – камера для топливного газа.
Даниель-Бок создал аналогичную конструкцию для сжигания бензина и другого углеводородного топлива.
Положительный электрод 60% FeO + 20%Fe3O4 + 20% шамотной глины.
Отрицательный электрод 60% FeO + 20%Fe опилки + 20% шамотной глины.
Смеси, смоченные в воде вмазывают в железный каркас, сушат и прокаливают при 800-900°С.
Твердый электролит готовят сплавлением при 1200°С, 43% Na2CO3, 27% моноцитового песка (3-4% ThO2 и 15-20% РЗМ), 20% WO3 + 10%Na2SiO3. удельное сопротивление при 700°С 3 Ом×cм, плотность тока 20 ма/см2, V=0,79В. Электроды практически не поляризуются.
При работе с газом 50% СО, 50%Н2, к.п.д. 80%. Недостатком является малая стойкость к изменению температуры пластины твердого электролита, приводящая к ее растрескиванию.
Необходимы катализаторы, ускоряющие электродные процессы при умеренных температурах и давлениях.
 2015-05-22
2015-05-22 3121
3121








