некоторых растворителей
| Растворитель | Эт, К×кг/моль | Кт, К×кг/моль |
| Вода | 0,51 | 1,86 |
| Этиловый спирт | 1,19 | – |
| Бензол | 2,63 | 5,1 |
| Диэтиловый эфир | 2,02 | 1,73 |
Понижение температуры замерзания раствора DТзам пропорционально моляльной концентрации раствора и выражается уравнением
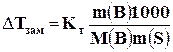 , (6)
, (6)
где DТзам – понижение температуры замерзания раствора, равное разности между температурой замерзания чистого растворителя Т0 и температурой замерзания раствора Тр: DТзам = Т0 – Тр; Кт – криоскопическая постоянная растворителя, характерная для данного растворителя и не зависящая от природы растворённого вещества. Криоскопическая постоянная растворителя показывает понижение температуры замерзания, которое соответствует раствору, содержащему 1 моль неэлектролита на 1000 г (1кг) растворителя. Единица К×кг/моль. Численные значения Кт для некоторых растворителей приведены в табл. 1; m(В) – масса растворённого вещества, г, М(В) – молярная масса растворённого вещества, г/моль;
m(S) – масса растворителя, г.
Пример 5. Для предотвращения замерзания в зимнее время различных разбавленных водных растворов к ним обычно добавляют глицерин (С6Н8О3). Вычислите, сколько граммов глицерина должно быть прилито к 100 г воды, чтобы раствор не замерзал до –5°С.
Решение. Молярная масса глицерина 92 г/моль. Для воды Кт = 1,86 К×кг/моль (см. табл. 1). Преобразуем уравнение (6) относительно массы растворённого вещества m(В)
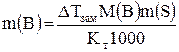 . (6а)
. (6а)
DТзам = Т0 – Тр = 273 – 268 = 5 К. Подставив цифровые значения в уравнение (6а), получим
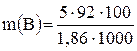 = 24,73 г.
= 24,73 г.
Чтобы раствор не замерзал до температуры –5 °С, надо к 100 г воды прилить 24,73 г глицерина.
Зависимость осмотического давления от объёма раствора, количества растворённого вещества и температуры выражается уравнением:
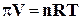 , (7)
, (7)
где p – осмотическое давление раствора, Па; v – объём раствора, м3; n – количество растворённого вещества, моль; R – газовая постоянная, равная 8,314 Дж/моль×К; Т – температура, К.
Заменив в уравнении (3) n/V, т.е. количество растворённого вещества в единице объёма, на С получим выражение:
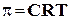 , (8)
, (8)
где С – молярная концентрация, моль/л.
Концентрация растворённого вещества С может быть выражена через массу растворённого вещества m(В) и его молярную массу М(В) г/моль. Тогда уравнение (8) примет вид:
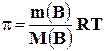 . (9)
. (9)
 2015-06-14
2015-06-14 3657
3657







