По физическим свойствам алкины напоминают алкены и алканы. Температуры их плавления и кипения увеличиваются с ростом молекулярной массы. В обычных условиях алкины С2–С3 – газы, С4–С16 – жидкости, высшие алкины – твердые вещества. Наличие тройной связи в цепи приводит к повышению температуры кипения, плотности и растворимости их в воде по сравнению с олефинами и парафинами. Физические свойства некоторых алкинов сведены в таблице.
Химические свойства
I. Реакции присоединения
1) Гидрирование. Гидрирование алкинов осуществляется при нагревании с теми же металлическими катализаторами (Ni, Pd или Pt), что и в случае алкенов, но с меньшей скоростью.
CH3–CєCH(пропин) ––t°,Pd;H2•® CH3–CH=CH2(пропен) ––t°,Pd;H2® CH3–CH2–CH3(пропан)
2) Галогенирование. Алкины обесцвечивают бромную воду (качественная реакция на тройную связь). Реакция галогенирования алкинов протекает медленнее, чем алкенов.
HCєCH ––Br2® CHBr=CHBr(1,2- дибромэтен) ––Br2® CHBr2–CHBr2(1,1,2,2- тетрабромэтан)
3) Гидрогалогенирование. Образующиеся продукты определяются правилом Марковникова.
CH3–CєCH ––HBr® CH3–CBr=CH2(2- бромпропен -1) ––HBr® CH3–CBr2–CH3(2,2- дибромпропан)
4) Гидратация (реакция Кучерова). Присоединение воды осуществляется в присутствии сульфата ртути. Эту реакцию открыл и исследовал в 1881 году М.Г.Кучеров.
Присоединение воды идет по правилу Марковникова, образующийся при этом неустойчивый спирт с гидроксильной группой при двойной связи (так называемый, енол) изомеризуется в более стабильное карбонильное соединение - кетон.
| C2H5–CєCH + H2O ––HgSO4® [C2H5– | C=CH2](енол) ® C2H5– I ø OH | C–CH3(метилэтилкетон) II O |
В случае гидратации собственно ацетилена конечным продуктом является альдегид.
| O II | ||
HCєCH + H2O ––HgSO4® [CH2=  Н Н
| CH](енол) ® CH3– I | C(уксусный альдегид) I |
| Вопрос 8, 9 конец. |
5) Полимеризация. Ацетиленовые углеводороды ввиду наличия тройной связи склонны к реакциям полимеризации, которые могут протекать в нескольких направлениях:
a) Под воздействием комплексных солей меди происходит димеризация и линейная тримеризация ацетилена.
HCєCH ––kat.HCєCH® CH2=CH–CєCH ––kat.HCєCH® CH2=CH–CєC–CH=CH2
b) При нагревании ацетилена в присутствии активированного угля (реакция Зелинского) осуществляется циклическая тримеризация с образованием бензола.
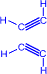
| + | 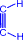
| ––600°C,C® | 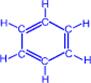
|
Применение
При горении ацетилена в кислороде температура пламени достигает 3150°C, поэтому ацетилен используют для резки и сварки металлов. Кроме того, ацетилен широко используется в органическом синтезе разнообразных веществ - например, уксусной кислоты, 1,1,2,2- тетрахлорэтана и др. Он является одним из исходных веществ при производстве синтетических каучуков, поливинилхлорида и других полимеров.
 2015-06-04
2015-06-04 519
519








